 产业资讯
产业资讯
 药智网
药智网  2025-08-16
2025-08-16
 1267
1267
7月药品注册受理与审批数据新鲜出炉!超千项申请中,化药仍是主力,中药创新提速,生物制品表现亮眼。例如,国产抗癌新药出海、经典名方现代化、儿童便秘中药新药、革命性口溶膜剂型……多领域创新成果涌现,审批效率提升,加速满足临床需求。
一起看看7月有哪些值得关注的新药动态!
01
受理情况
7月,CDE共受理药品注册申请1259个品种(受理号1666个)。按药品类型统计,化药仍为主体,达778个品种;中药287个品种;生物制品191个品种。
按审评任务类型统计,受理新药临床试验申请(以下简称IND)232个品种;新药上市许可申请(以下简称NDA)33个品种;同名同方药、仿制药、生物类似药上市许可申请(以下简称ANDA)316个品种;仿制药质量和疗效一致性评价注册申请(以下简称一致性评价申请)26个品种。
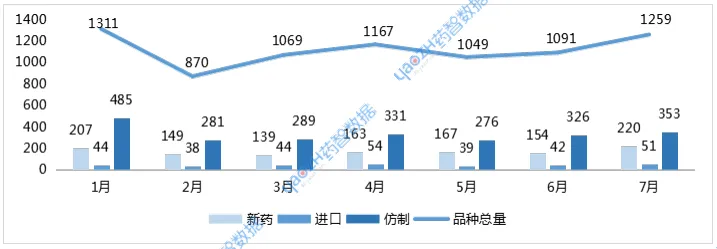
图1 2025年1-7月受理品种情况
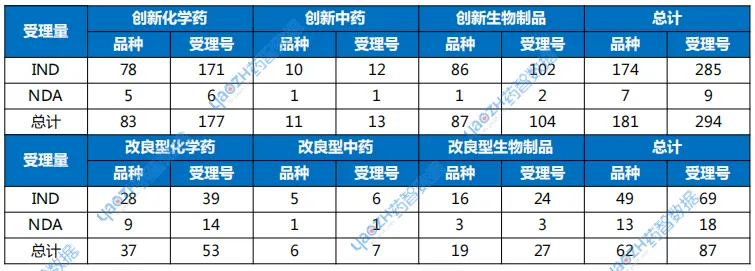
以注册分类统计,1类创新药受理181个品种。IND申请174个品种,NDA申请7个品种。2类改良型新药注册申请受理62个品种,化药申请37个品种,中药申请6个品种,生物制品申请19个品种。
亮点速览
•济川药业「小儿便通颗粒」源自陈永辉医生经验方,用于健脾和胃、行气导滞,专注儿童便秘。
•江苏威凯尔「安瑞替尼胶囊」——新一代国产泛癌种NTRK抑制剂,直击耐药,已被国家药监局纳入优先审评品种名单。
•先声药业携手康乃德引入「乐德奇拜单抗注射液」,全人源抗IL-4Rα单抗,瞄准特应性皮炎等Th2炎症。
•信诺维医药「注射用亚胺培南西司他丁钠福诺巴坦」——全球首个覆盖三大CRO的BL/BLI复方制剂,破局耐药菌“最后防线”。
•河南利欣制药的「柴胡鼻腔喷雾剂」以中药2.1类新药正式报产,项目已获河南省重点研发专项力挺,传统柴胡现代化再提速。
•上海艾力斯「甲磺酸伏美替尼片」——国产三代EGFR-TKI新适应症申请附条件上市:针对含铂化疗失败或不耐受、且携带EGFR 20外显子插入突变的局晚/转移性NSCLC成人患者,后续确证性试验将决定最终完全批准。
表1 2025年7月创新药与改良型新药注册申请受理情况
中药3类经典名方注册申请受理4个品种,为武汉康乐药业的真武颗粒,石家庄以岭药业的半夏白术天麻颗粒,合肥华润神鹿药业的宣郁通经汤颗粒,国药集团广东环球制药的芍药甘草颗粒。
3类化学仿制药注册申请受理125个品种,验证性临床申请10个品种,上市申请115个品种。4类化学仿制药受理228个品种。中药同名同方药受理1个品种,为包头中药有限责任公司申报的冠心丹参胶囊。生物制品3.3类生物类似药受理7个品种,其中预防用生物制品3个品种,治疗用生物制品4个品种。
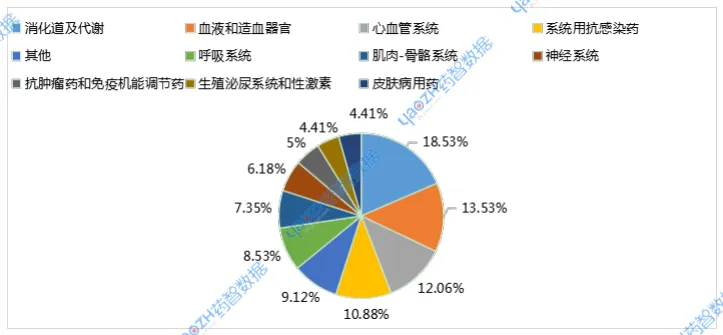
图2 2025年7月化学仿制药申报品种ATC分布情况
02
完成审批情况
NMPA完成审批1125个品种(受理号1482个),其中化药733个品种,中药221个品种,生物制品171个品种。以审评任务类型统计,IND申请完成审批175个品种,NDA申请27个品种,ANDA申请294个品种,一致性评价品种53个品种。按药智审评结论统计,批准临床238个品种,批准生产263个品种,批准进口16个品种,未被批准88个品种。
以注册分类统计,1类创新型新药完成审批141个品种,IND申请完成审批133个品种,NDA申请8个品种,临床批准率为98.5%,上市批准率为87.5%。2类改良型新药完成审批44个品种,IND申请完成审批37个品种,NDA申请完成审批7个品种,临床批准率为100%,上市批准率为71.45%。
新药上新
•妇科中药稀缺之作——参蒲颗粒(曾用名:参蒲盆安颗粒)获批上市!源自江苏省中医院谈勇教授临床经验方,专攻“盆腔炎性疾病后遗症-慢性盆腔痛(湿热瘀阻证)”。2021年至今,国内仅7款妇科中药新药获批,参蒲颗粒位列其中,创新含金量可见一斑。
•中国原研Bcl-2抑制剂“利沙托克拉片”重磅获批!通过阻断Bcl-2蛋白,重启癌细胞凋亡程序,对慢性淋巴细胞白血病(CLL)疗效明确且耐受性佳,并斩获FDA五项孤儿药资格认证,实力出海。
•齐鲁制药再添“口腔邮票”利培酮口溶膜——舌面一放,10余秒速溶,无需水服,方便吞咽困难患者。至此,齐鲁口溶膜家族已扩容至6款,剂型创新再下一城。
3类化学仿制药申请完成审批124个品种,批准临床5个品种,批准生产104个品种,未被批准15个品种。4类化学仿制药申请完成审批169个品种,批准临床6个品种,批准生产147个品种,未被批准17个品种。中药同名同方药完成审批的1个品种,为新疆维吾尔药业的通滞苏润江片,未被批准上市。3.3类生物制品生物类似药完成审评4个品种,批准临床3个品种,批准生产1个品种。
表2 2025年7月新药上市申请审评结论情况
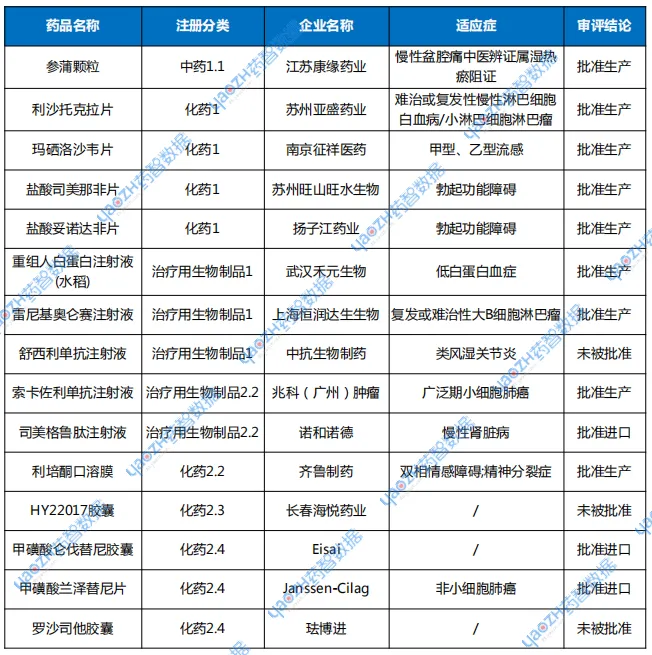
注:数据统计至2025年8月12日
03
优先审评与突破性治疗品种名单
CDE共将7个品种正式纳入优先审评。其中共计4个化药品种,3个生物制品品种,中药未有品种纳入优先审评。纳入优先审评理由涉及“附条件批准”“纳入突破性治疗药物程序”等。
突破性治疗品种名单有7个品种,同样也是4个化药品种,3个生物制品品种。涉及小细胞肺癌、慢性乙肝等适应症。
表3 2025年7月优先审评与突破性治疗品种名单
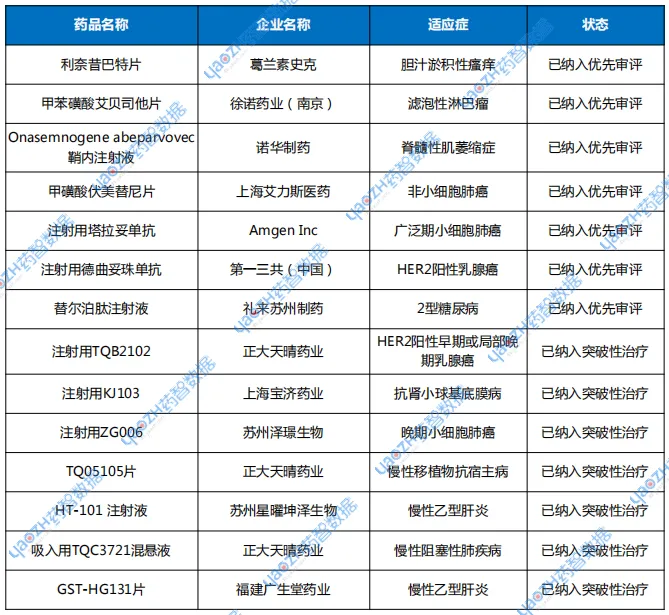
注:数据按公示日期进行统计
 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-05-07
2026-05-07
 78
78

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2026-05-07
2026-05-07
 108
108

 产业资讯
产业资讯
 药渡
药渡  2026-05-07
2026-05-07
 91
91
 热门资讯
热门资讯