 研发追踪
研发追踪
 药智数据
药智数据  2025-09-16
2025-09-16
 2613
2613
近日,CDE官网公示,康宁杰瑞/石药集团联合开发的HER2双特异性抗体KN026(安尼妥单抗注射液)新药上市申请(NDA)已获受理,适应症为“联合化疗用于HER2阳性胃癌二线治疗”。这是中国首个在该领域递交NDA的HER2双抗,也是全球范围内同机制药物中进度最快的一款。

图片来源:CDE 官网
该申请主要基于一项关键性II/III期临床研究(KC-WISE)的积极结果。研究显示,相较于对照组,KN026联合化疗在经曲妥珠单抗治疗失败的HER2阳性胃癌患者中,显著延长了无进展生存期(PFS)和总生存期(OS),且安全性良好。因其显著的临床价值,该药此前已被CDE授予突破性治疗药物资格,并于今年 8 月底获优先审评,审评进程有望加速。
目前,HER2阳性胃癌二线治疗领域尚无获批上市的抗HER2药物。临床医生在面对一线治疗失败的患者时,治疗选择非常有限。KN026作为中国首个在胃癌二线适应症中获得阳性结果的HER2双特异性抗体药物,有望填补这一临床空白,为患者提供新的生命希望。
KN026作为一款具有差异化价值的抗HER2双特异性抗体,其核心创新在于能同时结合HER2的两个不同表位,产生类似曲妥珠单抗与帕妥珠单抗的协同作用,从而增强信号阻断效果、提升抑瘤活性并潜在克服耐药。该产品精准瞄准了HER2阳性胃癌二线治疗缺乏标准抗HER2方案的临床空白,有望为曲妥珠单抗治疗失败的患者提供重要选择。此外,其在乳腺癌(III期)、结直肠癌等多瘤种领域的布局,展现了广阔的临床开发与市场拓展潜力。
KN026的研发历程体现了中国创新药企的持续深耕:
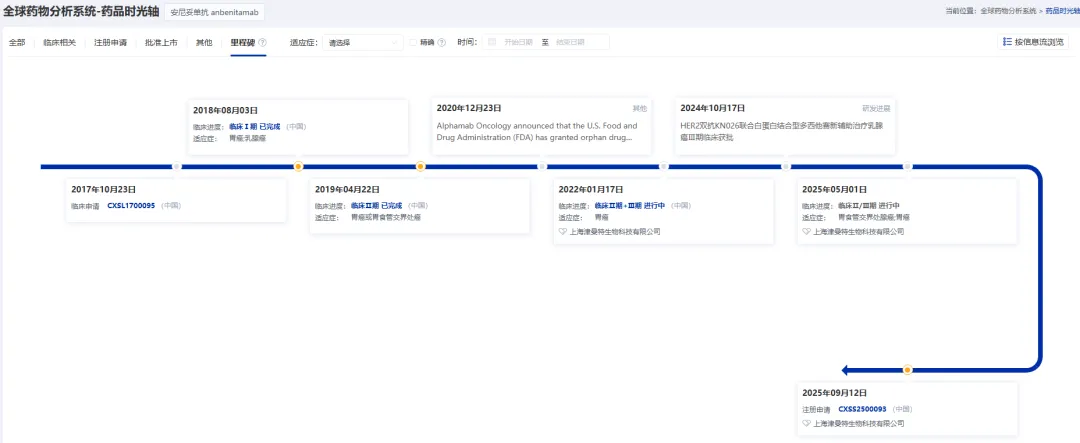
图片来源:药智数据企业版——全球药物分析系统
2017年10月:在中国提交临床申请,正式起步。
2018年08月:完成针对胃癌、乳腺癌的I期临床,初步验证安全性。
2019年04月:完成针对胃癌/胃食管交界处癌的II期临床,获得初步有效性证据。
2022年01月:针对胃癌的II/III期关键临床研究进行中,进入研发决胜阶段。
2025年09月:正式提交上市注册申请,迎来里程碑节点。
八年研发过程,见证了KN026从实验室走向患者,最终叩响市场大门的完整路径。
随着该产品进入优先审评,业界期待其能早日获批上市,为中国HER2阳性胃癌患者带来新的希望。同时,其在其他适应症的拓展也值得长期关注,有望成为中国创新药出海的一个潜在标杆。

 研发追踪
研发追踪
 新药界
新药界  2026-05-21
2026-05-21
 455
455

 研发追踪
研发追踪
 药智数据
药智数据  2026-05-21
2026-05-21
 571
571

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-05-18
2026-05-18
 592
592
 热门资讯
热门资讯