 产业资讯
产业资讯
 医药地理
医药地理  2026-03-25
2026-03-25
 5
5
3月23日,云顶新耀宣布与箕星药业达成资产收购协议 ,获得艾曲帕米鼻喷雾剂(拟定中文商品名:星必妥)在大中华区的开发、商业化及产品地产化权益。根据协议,云顶新耀将向箕星药业支付3000万美元首付款,以及最高不超过2000万美元的开发里程碑付款。毫无疑问,“倒爷”云顶新耀,这次又“倒买”下一个“超级大单品”。

不是“买爆款”,而是“买刚需”
在医药行业,产品是“1”,商业化是后面的“0”,没有“1”,一切都无从谈起。为何云顶新耀总能押中“蓝海大单品”?其选药的逻辑,不是“买爆款”,而是“买刚需”。
就拿这次引进的艾曲帕米鼻喷雾剂来说,这是一种新型、速效的钙离子通道阻滞剂,采用便携式鼻喷雾方式给药,起效迅速、耐受性良好,患者可居家自行使用,可及性较高,是FDA30多年来批准的首款且唯一获批用于成人阵发性室上性心动过速(PSVT)急性症状性发作的疗法。
而在中国,PSVT的患病率约为每1000人中有2.3至4人,估计患者总数达300万至600万。PSVT急性发作的治疗缺乏安全、便捷、可在院外自行使用的快速终止药物,使患者在发作期长期处于“被动等待”状态,缺乏真正意义上的“按需自救”工具。
PDB药物综合数据库显示,近三年国内PSVT相关药物国内销售金额已突破4.5亿元,且缺乏“特效药”,仅有钾通道阻滞剂胺碘酮、非二氢吡啶类钙通道阻滞剂(维拉帕米和地尔硫䓬)、腺苷等药物在急性期治疗中常被优先选用。正是基于这一临床痛点,云顶新耀在艾曲帕米鼻喷雾剂获得FDA批准后仅三个月,便迅速将其引入,印证了公司“买刚需”的判断逻辑。
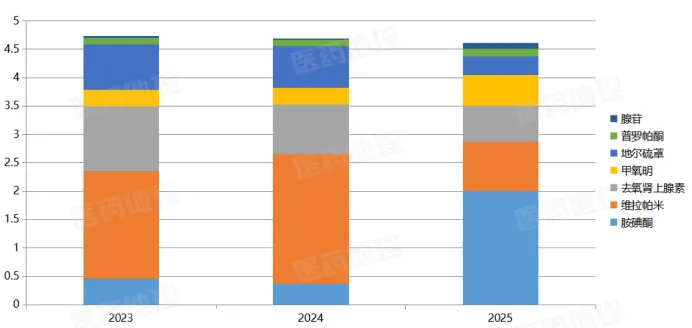
PSVT治疗药物国内销售份额(2023-2025)
来源:PDB药物综合数据库,中国医药工业信息中心
还有就是耐赋康(布地奈德肠溶胶囊),作为全球首个且唯一获批用于治疗原发性免疫球蛋白A肾病的口服靶向对因治疗药物,该药由云顶新耀通过独家授权引进并负责商业化。凭借靶向肠道黏膜B细胞的独特机制,这款“里程碑药物”从疾病源头减少致病性IgA1抗体的产生,成功填补了IgA肾病“无对因治疗药物”的临床空白。耐赋康于2024年11月成功纳入医保,在第一年便成为了十亿级大单品。
庞大的市场规模引来了不少企业争相抢夺首仿,去年年底,云顶新耀便陷入了和海南合瑞的“专利战”中十亿肾病药首仿之战!海南合瑞困于专利墙,齐鲁、石药正加速绕道。今年2月底,云顶新耀宣布专利诉讼取得积极进展:广州知识产权法院于2026年2月26日作出民事裁定书,全面支持公司提出的诉前行为保全申请,并责令相关仿制药企业立即停止侵权行为并停止挂网。

按照去年年底云顶新耀发布的公司战略发展及经营情况规划,公司将通过持续引进布局,在肾科、自身免疫、急重症、心血管/代谢及眼科等重点治疗领域,依靠科学及商业洞察力,形成“N+X”产品组合,抢抓蓝海大单品机遇。力争2028年收入突破100亿人民币,2030年突破150亿人民币。
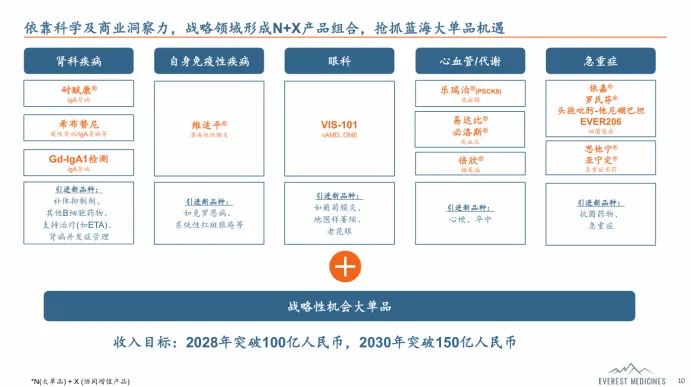
来源:云顶新耀官网
如何从“产品”到“商品”
如果说选品是眼光,那么商业化落地就是真刀真枪的硬仗。云顶新耀在这一阶段展现出的“执行力”和“精细化”,源于一套科学及商业洞察驱动的准入、医学、市场、销售一体化协同(AMMS)的商业化运营体系。
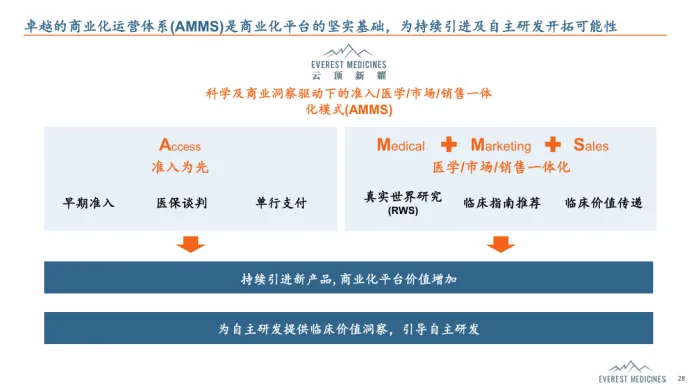
来源:云顶新耀官网
在传统药企的流程中,市场准入往往是上市后的“最后一公里”,但在云顶新耀的AMMS体系里,准入被前置到了产品上市之前,甚至临床开发阶段,从而打赢早期准入的“时间窗口战”。
以今年2月刚刚获批的自身免疫性疾病核心产品维适平(精氨酸艾曲莫德片)为例,早在2024年,该药物被纳入粤港澳大湾区内地9市临床急需进口港澳药品医疗器械目录,在大湾区率先实现临床应用,提前建立专家共识、积累真实世界数据。
3月9日,维适平获批后仅一个月就在中山大学附属第一医院开出首张处方。就在当天,广州、上海、杭州、西安、重庆、北京、南京7个核心城市的8家三甲医院同步开出首轮处方,互联网医院渠道也同步启动,以进一步扩大患者覆盖范围。这种“获批即落地、落地即放量”的节奏感,正是AMMS体系“准入前置”策略的直接体现。与此同时,云顶新耀表示将通过构建多渠道准入体系,提供多元化患者援助项目和创新支付方案,全力推动维适平纳入国家医保目录,提升该药物的可及性和可负担性,以满足巨大的临床需求。
此外,该药物已被纳入2024年美国胃肠病学协会(AGA)临床实践指南,推荐作为溃疡性结肠炎的一线治疗;并于2025年6月被纳入《2025 ACG 临床指南:成人溃疡性结肠炎》,获强烈推荐用于中重度活动性溃疡性结肠炎的诱导和维持治疗,从一个“可选项”变成了“标准方案”,市场放量将呈现指数级增长。
更重要的是,云顶新耀将供应链能力也纳入了商业化的早期规划。去年3月,即维适平获批前一年,云顶新耀就启动了嘉善工厂的本地化生产建设项目,支持维适平在大中华区及其他亚洲市场的持续供应。这种“产品未上市、工厂先投产”的前瞻性布局,确保了获批后能够迅速响应市场需求,避免因供应瓶颈错失放量窗口。
制药也是business
要在不确定中创造确定
曾几何时,License-in模式被资本市场戏称为“倒爷”,那些没有自研产品、单纯依赖引进的公司的估值逻辑一度受到强烈冲击,上市之路也困难重重。云顶新耀却用一套教科书级别的打法,向行业展示了另一种务实的生存哲学。
云顶新耀CEO罗永庆曾在接受媒体采访时坦言,自主研发就像“奢侈品”,并非每家企业都适合,也并非在发展的每个阶段都该选择。生物医药行业具有长周期、高投入、高风险、低成功率的特征,企业必须在不同阶段分散风险、寻找确定性。因此,构建自我造血能力至关重要,不能只依赖资本市场输血或银行贷款。而License-in,正是分散风险的有效路径之一。
在他看来,从引进入手搭建产品管线、实现早期收入,再逐步过渡到自主研发,是一条风险更小、更务实的路径。他指出,自己从头干到尾固然勇气可嘉,但要面对现实,尤其在今天的大环境下。制药业终究是一门生意,要盈利、要规避风险、要确定性。
云顶新耀的故事启示我们:商业化能力本身就是一条难以复制的护城河,不仅能将“好药”转化为“好卖的药”,更能在行业寒冬中通过对外输出服务反哺研发,实现穿越周期的自我造血。
其次,“以商养研”是比单纯烧钱更可持续的发展路径,通过引进成熟产品快速构建商业化能力和稳定现金流,再反哺自研前沿技术,方能实现从“License-in”到“自研创新”的平滑过渡。
最后,药企的竞争已从单品竞争升级为全生命周期管理能力的竞争,只有打通临床开发、注册上市、医保准入到病程全覆盖的每一个环节,才能在复杂多变的医疗市场中建立真正的壁垒。

 产业资讯
产业资讯
 动脉网
动脉网  2026-03-25
2026-03-25
 5
5
 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2026-03-25
2026-03-25
 5
5

 产业资讯
产业资讯
 同写意
同写意  2026-03-25
2026-03-25
 5
5