 研发追踪
研发追踪
 Insight数据库
Insight数据库  2025-03-10
2025-03-10
 3576
3576
3 月 5 日,罗氏宣布,美国 FDA 已接受该公司奥妥珠单抗 (Obinutuzumab,Gazyva/Gazyvaro) 用于治疗狼疮性肾炎的补充生物制品许可申请 (sBLA)。FDA 预计将在 2025 年 10 月之前做出审批决定。奥妥珠单抗此前已获批治疗多种淋巴瘤适应症,本次是该药递交的首个非肿瘤适应症上市申请。

截图来源:罗氏官网
狼疮性肾炎是一种使人衰弱并可能危及生命的疾病。在狼疮性肾炎中,致病的 B 细胞会引发持续性炎症,从而损害肾脏。
奥妥珠单抗是一种靶向 CD20 抗体,可通过靶向致病的 B 细胞帮助更好地控制疾病,保护肾脏免受进一步损害,并可能预防或延缓进展为终末期肾病。2019 年,根据 II 期 NOBILITY 研究的数据, FDA 已授予该药治疗狼疮肾炎的突破性疗法认定。
此次上市申请是基于 III 期研究 REGENCY(NCT04221477)的积极结果。该研究结果已于 2025 年 2 月在世界肾脏病大会 (WCN) 上同时公布,并发表在《新英格兰医学杂志》上。
数据显示,REGENCY 研究达到了其主要终点;与单纯标准治疗相比,接受奥妥珠单抗联合标准治疗的患者中,近一半的患者实现了完全肾脏缓解 (CRR),具有统计学意义和临床意义的改善。在研究中,接受奥妥珠单抗联合标准治疗的患者中,46.4% 在 76 周时实现了 CRR,而单纯接受标准治疗的患者中,这一比例为 33.1%。
此外,研究还显示,患者补体水平也得到了临床意义的改善,抗 dsDNA、疾病活动和炎症的标志物也得到了降低。预先指定的亚组分析显示,患者亚组均具有一致的 CRR 益处。奥妥珠单抗的安全性与其血液肿瘤学适应症中观察到的良好特征一致。
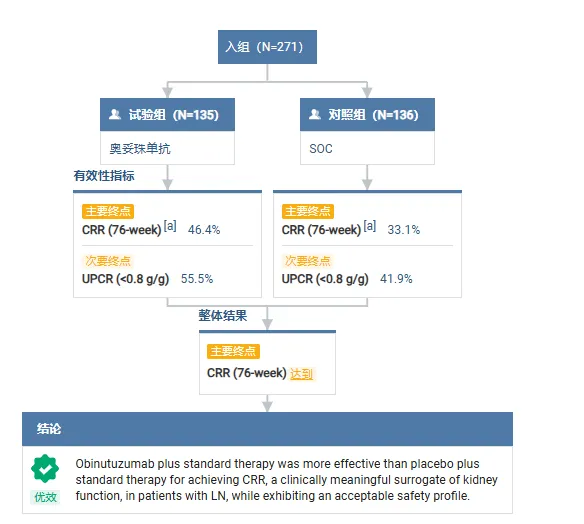
来源:Insight 数据库
罗氏在新闻稿中指出,奥妥珠单抗是随机 III 期研究中唯一一种证明 CRR 对狼疮性肾炎有益的抗 CD20 单克隆抗体。该公司还计划基于 III 期 REGENCY 研究的数据向欧洲 EMA 递交奥妥珠单抗该适应症的上市申请。
除了 REGENCY 研究,罗氏还在评估奥妥珠单抗治疗患有狼疮性肾炎的儿童和青少年、膜性肾病患者、儿童期特发性肾病综合征和系统性红斑狼疮的效果和安全性。
奥妥珠单抗之外,罗氏在免疫性肾脏和相关疾病领域的产品线还包括:
Sefaxersen,一种靶向补体因子 B(CFB)的反义寡核苷酸疗法,正在开展用于原发性免疫球蛋白 A 肾病 (IgA 肾病) 且进展风险较高患者的 Ⅲ 期临床;
莫妥珠单抗(Mosunetuzumab),一种 CD20xCD3 T 细胞接合双特异性抗体,正在研究用于系统性红斑狼疮;
可伐利单抗(Crovalimab),一种靶向 C5 的新型循环单克隆抗体,正在开展用于非典型溶血性尿毒症综合征的 Ⅲ 期临床;
RG6382,一种 CD19xCD3 T 细胞接合双特异性抗体,正在开展用于系统性红斑狼疮的Ⅰ期临床;
以及 P-CD19CD20-ALLO1,一种同种异体 CD19 × CD20 双靶点 CAR-T,拟开发用于系统性红斑狼疮、多发性硬化适应症。
原文链接:
https://www.roche.com/media/releases/med-cor-2025-03-05

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-05-18
2026-05-18
 346
346

 研发追踪
研发追踪
 医药魔方Info
医药魔方Info  2026-05-18
2026-05-18
 412
412

 研发追踪
研发追踪
 药研网
药研网  2026-05-18
2026-05-18
 327
327
 热门资讯
热门资讯