 研发追踪
研发追踪
 创药邦
创药邦  2025-09-01
2025-09-01
 2428
2428
2025 年 8 月 27 日,医疗界传来重磅喜讯!ExCellThera 子公司 Cordex Biologics 研发的创新型血癌干细胞疗法Zemcelpro®(UM171 细胞疗法) ,成功斩获欧盟委员会(EC)的条件性上市许可。这一里程碑式进展,为无数深陷血癌困境的患者,点亮了新的生命希望!

一、血癌患者的 “生死困境”:供体短缺成治愈拦路虎
在欧洲,每年有超10,000 名患者被确诊为需要干细胞移植的血液恶性肿瘤,白血病、骨髓增生异常综合征等疾病正无情吞噬生命。
尽管近年来干细胞移植技术不断进步,可移植的 “可及性” 有所提升,但残酷的现实是:
大量患者因找不到兼容的供体,或无法在短时间内获取所需细胞,只能眼睁睁错过最佳治愈时机。
每一个数字背后,都是一个在病痛中挣扎的生命,一个期盼奇迹的家庭 —— 供体短缺,早已成为横亘在患者与健康之间的 “生死鸿沟”。
二、Zemcelpro®:为 “无供体” 患者量身定制的 “生命解药”
作为一款一次性、个性化的细胞疗法,Zemcelpro® 就像为 “无供体” 患者量身打造的 “救星”,其核心创新点,彻底打破了传统干细胞移植的局限:
1. 原料创新:从脐带血中 “挖潜力”
Zemcelpro® 的干细胞来源并非传统的骨髓或外周血,而是捐赠者的脐带血。研发团队通过特殊技术,对脐带血中的一部分干细胞进行培养和增殖,让原本 “量少力弱” 的脐带血干细胞,焕发出更强的治疗能力。
2. 成分精妙:两种细胞 “协同作战”
Zemcelpro® 包含两大关键成分,且均来自同一个脐带血单位,避免了多来源细胞的排斥风险:UM171 扩增的 CD34 + 细胞(dorocubicel) :经过特殊分子 UM171 处理,数量大幅增加,是重建患者造血功能的 “主力部队”;未扩增的 CD34 - 细胞 :辅助 “主力部队” 发挥作用,提升干细胞在患者体内的存活和定植能力。这种 “1+1>2” 的组合,让一个小型脐带血单位的干细胞 “脱胎换骨”,足以满足患者的移植需求,彻底解决 “细胞不够用” 的难题。
3. 适用精准:聚焦 “最急需” 的患者
此次欧盟批准的 Zemcelpro®,适用人群非常明确:需要接受清髓性预处理(化疗或放疗)后,进行同种异体造血干细胞移植的成人血液恶性肿瘤患者,且这些患者无法获得其他类型的合适供体细胞。简单来说,就是那些 “走投无路” 的患者 —— 传统移植路走不通,却能通过 Zemcelpro® 获得治愈机会。
4. 疗效硬核:临床数据 “说话”
疗效好不好,数据是最好的证明!ExCellThera 对两项单臂、开放标签研究的汇总分析显示:参与研究的 25 名患者中,有21 名(占比 84%)在中位 20 天内成功实现中性粒细胞植入。这一关键指标意味着:供体干细胞已在患者体内成功 “落地生根”,开始生成白细胞中性粒细胞 —— 这是患者免疫系统重建的重要标志,也是治疗成功的核心第一步!
三、欧盟 “有条件批准”:为何 “未完善数据” 仍能获批?
很多人会疑惑:为何欧盟会给 Zemcelpro®“有条件上市许可”?其实,这背后藏着对 “未满足医疗需求” 的迫切回应。
什么是 “条件性上市许可”?欧盟的 “条件性上市许可”,专门授予那些能解决重大未满足医疗需求的药物:比如治疗严重危及生命的疾病(如血癌),且目前缺乏令人满意的治疗方法;或新疗法能提供 “重大治疗优势”。
在这种情况下,即便药物的 “全面临床数据尚未完全完善”,但它为患者带来的 “救命益处”,远大于对 “未来数据补充” 的等待 —— 简单说,就是 “先让患者用上药,再持续完善证据”。
此次批准的意义:不止是 “一款药上市”
Zemcelpro® 的获批,不仅是为 “无供体” 血癌患者打开了一扇门,更向整个医疗界传递了一个信号:针对 “难治性、罕见性” 疾病的创新疗法,将得到更灵活、更务实的监管支持 —— 患者的 “生命需求”,永远是第一位的。
四、全球布局:从欧洲出发,让更多患者 “有药可用”
ExCellThera 并未止步于欧盟市场,而是早已启动 “全球救急” 计划:
1. 多国监管申请同步推进
目前,公司已计划在美国、加拿大、英国、瑞士等国家和地区提交 Zemcelpro® 的监管申请,争取让这一疗法尽快惠及更多国家的血癌患者。
2. 商业化合作加速落地
为了让 Zemcelpro® 在欧洲及其他市场更快 “触达患者”,Cordex Biologics 正积极寻求战略合作伙伴关系,通过整合全球医疗资源,缩短 “从获批到临床应用” 的时间差。
3. 研究升级:覆盖更多患者群体
除了推进现有适应症的商业化,公司还计划:尽快启动关键 III 期临床研究,进一步验证 Zemcelpro® 的长期疗效和安全性;探索疗法在儿科患者、非恶性血液疾病患者中的潜在应用 —— 未来,可能有更多类型的患者,能从这一技术中受益。
五、背后的 “技术王者”:ExCellThera 如何引领行业?
Zemcelpro® 的成功,离不开 ExCellThera 在 “增强型血干细胞疗法” 领域的深耕 —— 这家公司,早已是全球该领域的 “技术标杆”。
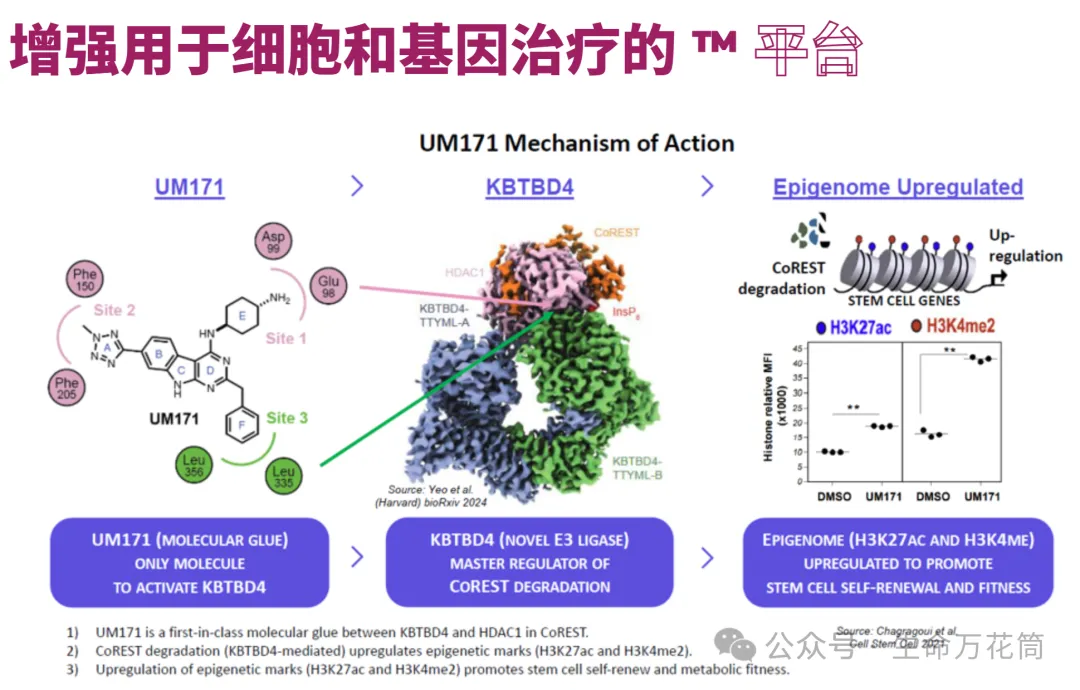
ExCellThera公司在增强型血干细胞疗法领域是全球领导者。其专有的Enhance™平台专注于细胞扩增和代谢适应性,旨在通过扩增任何来源的造血干细胞(HSCs)并抵消培养或基因编辑引起的应激效应,从而提供更高剂量的功能性治疗性干细胞 。UM171分子作为Zemcelpro®的核心技术,具有一流的体外扩增和HSCs代谢适应性作用机制。
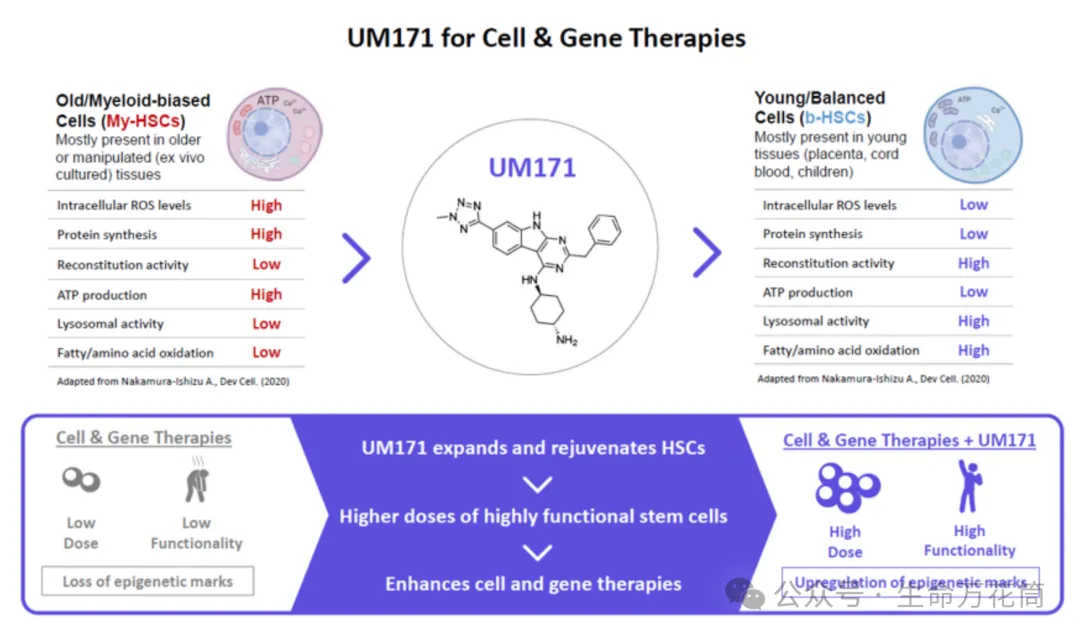
其核心竞争力,来自专有的Enhance™平台:这一平台专注于 “细胞扩增” 和 “代谢适应性” 两大关键技术,能实现两大突破:高效扩增:无论干细胞来源是脐带血、骨髓还是外周血,都能通过平台技术大幅提升细胞数量;减少损伤:抵消细胞在培养或基因编辑过程中产生的 “应激效应”,确保最终用于治疗的干细胞,保持 “高活性、高功能性”。
而 Zemcelpro® 的核心技术 ——UM171 分子,更是平台的 “王牌”:它具备 “一流的体外扩增能力” 和 “造血干细胞代谢适应性调节作用”,能在不损伤干细胞 “干性” 的前提下,让细胞数量和活性双提升 —— 这也是 Zemcelpro® 能突破传统疗法局限的关键所在。
一次获批,一场 “血癌治疗” 的新革命
Zemcelpro® 获欧盟批准,不仅是 ExCellThera 的 “里程碑”,更是全球血癌治疗领域的 “突破性进展”。它打破了 “无供体 = 无治愈希望” 的魔咒,为无数患者点亮了生命之光;也为 “个性化细胞疗法” 的发展,提供了 “从实验室到临床” 的成功范本。
未来,随着更多国家的获批、更多临床研究的推进,相信 Zemcelpro® 会书写更多 “生命奇迹”,为人类对抗血癌的 “战争”,增添一枚强有力的 “武器”!让我们共同期待:那一天早日到来 —— 所有血癌患者,都能不再因 “供体” 而绝望,都能拥有 “重生” 的机会!
英文链接:

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-05-18
2026-05-18
 404
404

 研发追踪
研发追踪
 医药魔方Info
医药魔方Info  2026-05-18
2026-05-18
 468
468

 研发追踪
研发追踪
 药研网
药研网  2026-05-18
2026-05-18
 381
381
 热门资讯
热门资讯