 产业资讯
产业资讯
 BiG生物创新社
BiG生物创新社  2025-11-25
2025-11-25
 820
820
每一天,全球众多1型糖尿病患者都在进行着一场精密的“计算”:指尖采血,测量血糖,注射胰岛素,计算碳水……这不仅是他们维系生命的仪式,更是一场与自身免疫系统无休止的谈判。自1921年胰岛素被发现以来,这根生命的绳索将无数人从死亡的边缘拉回,但它并非治愈的方舟。一个世纪过去了,人们依然在问:这场与自己身体的漫长战役,终点究竟在何方?
然而,今天我们正站在一个历史性的拐点。生物技术的浪潮正以前所未有的力量,拍打着医学的边界。基因编辑、细胞疗法、免疫调控……这些曾经只存在于科幻小说中的技术,如今已在我们眼前汇聚成一道清晰的曙光。人们不再仅仅满足于“管理”疾病,而是开始郑重地谈论“根治”的愿景。在这样的时代大背景下,MNC的战略部署对于1型糖尿病彻底被攻克的目标至关重要,而在MNC之中,截然相反的道路却在悄然铺开。
诺和诺德最近宣布了终止其细胞疗法部门,撤出“治愈”1型糖尿病的干细胞项目;而赛诺菲几乎同时与美国EVOQ Therapeutics签署总额最高达5亿美元的合作协议,押注于通过免疫耐受重建恢复机体平衡的新路径。
两家胰岛素国际巨头,在一退一进之间,展现了科学与现实的分叉口。一个百年前被胰岛素改写命运的疾病,是否仍有摆脱依赖、走向治愈的可能?
01
百年胰岛素的未竟之业
1型糖尿病(T1D)是一种典型的自身免疫性疾病。患者的免疫系统错误地将胰腺中的胰岛β细胞视为外来抗原,持续攻击并破坏它们,导致胰岛素分泌能力永久丧失。研究认为,遗传易感性与环境因素共同触发了这场免疫风暴:特定HLA基因型人群在病毒感染或肠道菌群紊乱等刺激下,T细胞耐受机制被打破,疾病一旦启动便几乎不可逆转。
1921年胰岛素的发现,让糖尿病从致命疾病变为可管理的慢病。一个世纪以来,胰岛素制剂从动物源进化为重组人胰岛素,再到超速效与长效修饰剂型。如今,胰岛素泵与连续血糖监测(CGM)的结合,使“人工胰腺”成为现实雏形。截至2025年,FDA已批准多款闭环胰岛素输注系统(如Medtronic MiniMed 780G与Tandem Control-IQ),虽能部分自动调节胰岛素剂量,但仍需人工输入餐食信息,而且这一体系仍属于生理替代而非病理修复,它维持血糖稳定,却无法恢复内源性胰岛功能。
目前的标准治疗仍以胰岛素替代为核心,通过每日注射或泵输注控制血糖波动,辅以实时监测与饮食、运动管理。部分GLP-1受体激动剂或SGLT2抑制剂正在探索辅助使用,但疗效与安全性尚未确立,目前未被主流指南推荐,仅在特定病例或研究性使用中考量,且多为非一线/非标准治疗。对患者而言,这种治疗意味着终身依赖:在胰岛素中断后可迅速进展为酮症酸中毒,尤其在儿童与急性感染等诱因下进展更快。
据国际糖尿病联盟估算,全球约有800万名T1D患者,占全部糖尿病的不到一成,却承担着最高的管理负担。他们多在儿童或青年时期开始发病,也可见于成年人,需要每日注射或佩戴设备维持生命。高收入国家的技术革新显著改善了生存质量,但在低收入地区,胰岛素可及性仍然是威胁生命的现实问题。
胰岛素的发明拯救了无数生命,却未让疾病真正痊愈。它极大延长了患者寿命,却未能解除对外源胰岛素的长期依赖。如何重建被免疫系统摧毁的胰岛功能,成为这一百年未竟的科学命题。
02
诺和诺德T1D细胞疗法激流勇退为哪般?
2025年10月,诺和诺德正式关闭其细胞疗法部门。这一决定意味着公司全面退出细胞疗法领域,而不仅仅是终止1型糖尿病项目。该部门此前负责三条主要研发线:包括治愈1型糖尿病的干细胞疗法、与日本Heartseed合作的心衰干细胞项目,以及由学术机构主导的帕金森病细胞疗法。根据报道,诺和诺德计划裁撤约250名员工,并寻求合作方继续推进部分资产。
这一调整是新任首席执行官Mike Doustdar推行的全球重组计划的一部分,削减约11%的员工,将节约的成本重新投入高回报的代谢疾病主线。就在同一周,诺和诺德宣布以52亿美元收购Akero Therapeutics,强化在代谢功能障碍性脂肪性肝炎(MASH)领域的布局。对于一家在GLP-1药物推动下快速获取大量现金流的企业来说,这一策略转向几乎是必然的:继续扩大肥胖和代谢药物市场占有,而非在高风险、长期难以商业化的“治愈型”细胞疗法上押重注。
诺和诺德的细胞疗法探索始于上个十年,由细胞生物学家Jacob Sten Petersen领导。他后来升任公司全球研发主管,也是在内部邮件中亲自宣布了部门关闭。这个项目原本承载着极高的科研理想,即利用多能干细胞(pluripotent stem cells)分化出具胰岛β细胞功能的细胞群,移植入患者体内以恢复内源性胰岛素分泌。其原理与Vertex的VX-880/VX-264颇为相似:通过体外分化生成成熟的胰岛细胞,再注入肝门静脉或皮下空间,在宿主血管系统中重建“人工胰岛”。
早期动物实验显示,这些细胞可以在短期内分泌胰岛素并改善血糖耐量,但难以维持长期功能。最大障碍来自两个方面:一是制造一致性。干细胞分化过程极为复杂,批次间差异大,任何细微工艺变化都可能导致成熟度和分泌能力下降;二是免疫排斥。异源细胞极易被宿主免疫系统清除,而封装材料虽能隔离免疫攻击,却常导致氧供不足、细胞坏死或装置失效。诺和诺德曾尝试过免疫隔离封装等装置/材料学途径以在免疫保护与营养供给之间求取平衡,但未能在安全性与有效性之间找到可行平衡。
到2023年,FDA批准了美国CellTrans公司的Lantidra(donislecel),成为首个针对1型糖尿病的细胞疗法。这一事件在业界被视为“概念验证”的成功,也间接凸显了诺和诺德所面临的现实鸿沟。
Lantidra的机制源自异体胰岛移植。研究人员从器官捐赠者的胰腺中分离出胰岛细胞群,经质量检测与制备后注入患者肝门静脉,使其在体内重新定植并分泌胰岛素。FDA的批准适应症极为限定:仅适用于那些在标准治疗下仍反复出现严重低血糖、且无法通过胰岛素调整或血糖监测维持稳定的成年患者。换言之,这是一种针对“管理失灵型”1型糖尿病的最后手段,而非面向普通患者的常规疗法。
在两项开放标签的研究中,共有30名患者接受了一至三次胰岛细胞注射。结果显示,其中21名受试者在至少一年内无需外源性胰岛素,其中11人保持1至5年,另有10人时间更长。但疗效存在个体差异,部分患者在随访中重新出现血糖波动。为了防止排斥,所有受试者均需长期服用免疫抑制剂,这带来了感染、肝肾毒性等严重风险。FDA在批准时特别强调,Lantidra必须在专业中心施行,其风险与获益应逐案评估。
然而,Lantidra并非真正的再生疗法,它依赖长期免疫抑制药物维持移植物存活,且每批制剂都需要供体胰腺,供给极其有限。换言之,这是一种“替代性移植疗法”,而非“再生性治愈”。其机制是补充外源细胞,而不是让患者自身重新生成β细胞。成本与供体资源则是另一重限制。每一疗程依赖合适的胰腺供体,制造和管理费用高昂,单次移植成本达数十万美元,且需终身免疫抑制维持。保险机构尚未形成稳定的报销政策,这使Lantidra更像是一个“技术可行性验证”的产品,而非可普及的商业疗法。
诺和诺德的项目则试图跳过供体瓶颈与伦理限制,通过干细胞体外制造实现无限供应,并最终摆脱免疫抑制依赖,这正是其被称为“治愈型细胞疗法”的原因。但这一路线在科学上更复杂,在产业上更昂贵。相比之下,Lantidra虽然已获批,却更像一项技术原型:它证明了“外源胰岛可以起效”,也暴露了“移植无法普及”的现实。
从战略视角看,诺和诺德的撤退并不是科学的失败,而是商业结构的重整。细胞疗法的开发周期长、监管标准未定、制造体系尚不成熟,与公司当前高增长、高盈利的代谢药物主线不再契合。正如Petersen在接受丹麦媒体采访时所言:“我们能在实验室复制自然,但尚不能在工业规模复制自然。” 这句话既是科学家的遗憾,也是企业家的现实。
因此,诺和诺德关闭细胞疗法部门的决定,既是对科学边界的承认,也是一种战略止损。它放弃的不是治愈的理想,而是现阶段无解的商业模式。对整个行业而言,这一撤退提醒人们:1型糖尿病的治愈并非不可能,但要跨越科学与可及性之间的深渊,仍需更漫长的旅程。
03
赛诺菲的回归
重建免疫耐受的尝试
就在诺和诺德正式退出细胞疗法赛道的同一周,另一家胰岛素巨头赛诺菲则踏上了另一条通向治愈T1D的道路。2025年10月16日,美国生物技术公司 EVOQ Therapeutics 宣布与赛诺菲达成总额最高 5 亿美元的全球合作与许可协议。根据双方声明,这一合作将围绕 EVOQ 的专有 NanoDisc 平台展开,这是一种重建机体免疫耐受(immune tolerance)的新型免疫调控技术。赛诺菲将负责后续临床开发与全球商业化,而 EVOQ 将获得分级里程碑金与销售分成。
这一消息在糖尿病研究圈引起广泛关注。因为 EVOQ 所定义的技术目标,不再是“替换被破坏的胰岛细胞”,而是让免疫系统重新学会不要错误地攻击它们。它代表着一种与诺和诺德截然不同的治愈逻辑,从细胞外的“修复”转向免疫内的“重编程”。
1型糖尿病的核心病理是免疫系统错误地识别胰岛β细胞抗原(如胰岛素前体、GAD65、IA-2等)为外来物,并持续攻击。这种错误源于树突状细胞(dendritic cells, DCs)在抗原呈递环节的偏差:在健康个体中,树突状细胞会将胰岛抗原呈递给T细胞,并传递“自我”信号,诱导其保持静默状态;而在自身免疫患者中,这一耐受过程被破坏,DCs 反而激活T细胞,启动破坏性免疫链条。
EVOQ 的 NanoDisc 平台正是针对这一环节设计。它利用一种基于合成高密度脂蛋白(synthetic HDL)的纳米盘结构(直径约 10–12 nm),将疾病相关抗原与免疫调节小分子共同包裹,精准递送至树突状细胞。HDL 颗粒天然能被 DCs 的清道受体(如 SR-B1、CD36)识别并摄取,因此这一系统能高效进入目标细胞。
进入 DCs 后,NanoDisc 中的抗原以“自我”信号形式呈递给T细胞,同时辅以免疫调节分子抑制共刺激信号,从而诱导调节性T细胞(Tregs)增生,重建对自身抗原的免疫耐受。简而言之,它不是全局性免疫抑制,而是一种抗原特异性的“免疫重教育”。
EVOQ 在动物模型中已验证了该机制。在NOD(非肥胖糖尿病)小鼠实验中,注射胰岛抗原-NanoDisc的动物中有超过70%未发展为糖尿病,而对照组几乎全部发病。组织切片显示,胰岛中残余β细胞数量显著增加,血糖长期稳定。这些结果发表于2024年《Nature Biomedical Engineering》,并被认为是迄今最接近“功能性免疫耐受”的实验之一。
传统免疫抑制药物(如类固醇、钙调磷酸酶抑制剂或抗CD3抗体)通过系统性削弱免疫活性来减少自身组织攻击。它们确实可以延缓病程,但代价是感染风险上升、肿瘤发生率增加、长期副作用严重。相反,EVOQ 的 NanoDisc 平台力图仅在涉及病理抗原的通路上发挥作用,让机体重新区分“自我”与“非自我”,恢复免疫稳态,而非简单压制免疫系统。
如果这种策略在人体中得以验证,它将代表一种“治愈性免疫疗法”的范式转变:患者无需补充胰岛细胞,也无需终身用药,而是通过一次或有限次免疫重塑,实现长期缓解。EVOQ在新闻稿中将该平台定位为有望带来“潜在治愈性”的自身免疫疗法,反映了他们对这一方向的高度期待。
选择EVOQ的NanoDisc平台,既是一种科研合作,也是一次价值观转向:与其在胰岛细胞替代上复制昂贵的细胞疗法路径,不如从病理源头纠正免疫错误,构建可规模化、可支付的治疗模式。理论上,这种疗法若成功,可像疫苗一样通过注射递送,避免昂贵的制造与手术过程。
尽管概念令人振奋,但NanoDisc技术距离临床应用仍有长路。首先是抗原选择的个体差异:不同患者的自身免疫靶点并不完全相同,若要实现精确耐受,需要个体化抗原组合。其次是免疫记忆的稳定性:在停止治疗后,是否能长期维持耐受状态仍缺乏验证。此外,递送系统的安全性和可制造性也需通过临床验证。
但赛诺菲的押注有其逻辑。对于一个全球免疫疾病管线布局广泛、具备成熟开发体系的制药巨头来说,EVOQ的技术不仅是科研投资,更是未来治愈T1D的彻底疗法。相较于诺和诺德在细胞层面构筑人工胰岛,赛诺菲试图在免疫层面“重启生理容忍”。
在胰岛素问世百年之后,科学的焦点正从替代走向重编:不再单纯补足缺失,而是让身体重新学习如何与自身和解。
04
从替代到重编
T1D治愈轮廓显现
当诺和诺德的实验室灯光熄灭、赛诺菲的免疫研究重新点亮时,人类在追寻1型糖尿病“治愈”的道路上,其实只走完了一个循环。百年前,胰岛素的发现将死亡推开;百年后,我们又一次在尝试,不再仅仅维持生命,而是要让身体重获自我调节的能力。
这一轮科学探索的意义,并非立刻让胰岛素消失于历史,而在于揭示了治愈的真正含义:它不只是生理的恢复,更是系统的重建。Lantidra证明在严格限定人群并配合长期免疫抑制的前提下,外源胰岛细胞可实现阶段性胰岛素独立,但高成本、供体稀缺与免抑风险限制了普及。诺和诺德的撤退显示干细胞疗法的科学可行,却也暴露出产业化与支付体系的瓶颈;赛诺菲与EVOQ的合作则提示另一种希望,或许治愈并不需要移植,而是让免疫系统重新识别自己。
科学正在从“替代”走向“重编”,从对症修补转向对因矫正。真正的治愈,也许不在于外部干预的强度,而在于机体重新获得平衡的能力。对1型糖尿病而言,这意味着免疫容忍的恢复、β细胞的保存、替代或重建、以及一个可以持久维系的内源性稳态系统。
然而,这条路依然漫长。免疫重建的复杂性远超单一药物机制,干细胞疗法的可制造性与安全性仍待时间检验。更根本的问题在于:即便科学成功,能否实现可负担、可及的应用?Lantidra的案例已经揭示了现实差距。一个疗法可以被批准,却难以被普及。治愈的定义若只存在于极少数人的临床奇迹,而无法转化为公共健康的成果,它就仍不完整。
在这个意义上,诺和诺德的撤退与赛诺菲的入场并不是胜负的对照,而是科学的接力:前者验证了生物工程的极限,后者重新启动了免疫逻辑的可能。它们共同塑造了一个轮廓:1型糖尿病的治愈将不会来自某一个突破,而是来自细胞替代与免疫重编的交汇,来自技术、制度与伦理的协同作用。
也许我们仍然需要很长时间才能真正摆脱胰岛素,但科学已经证明,这一目标并非不可实现。治愈的关键或许不在于找到某一种药物,而在于重新认识这种疾病本身,理解它如何产生,如何被身体误解,以及如何恢复平衡。当我们能够让免疫系统重新容忍自身,维持正常的胰岛功能,治愈将不再是遥远的理想,而是一个可以逐步实现的医学目标。
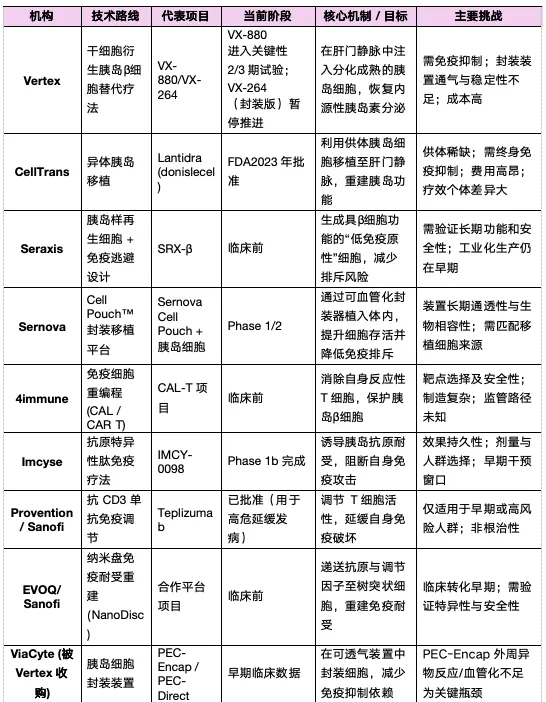
附表. 全球主要1型糖尿病治愈性疗法管线概览


 产业资讯
产业资讯
 医药魔方Info
医药魔方Info  2026-05-04
2026-05-04
 126
126

 产业资讯
产业资讯
 药融圈
药融圈  2026-05-04
2026-05-04
 123
123

 产业资讯
产业资讯
 Medaverse
Medaverse  2026-05-04
2026-05-04
 124
124
 热门资讯
热门资讯