 产业资讯
产业资讯
 医药地理
医药地理  2026-01-30
2026-01-30
 256
256
近日,FDA药品评价与研究中心(CDER)发布了《2025年新药治疗审批报告》,揭示了过去一年在药物创新、审批效率与可及性方面的关键进展。

根据报告,2025年CDER批准了46个新药,其中首创新药(FIC)占比高达43%。这一数据显示出美国医药行业在创新疗法开发上的强劲势头。罕见病治疗领域更是创下历史纪录,获批新药中有50%是针对罕见疾病的疗法,平均每两个新药中就有一个聚焦于小群体患者的医疗需求。更引人注目的是,72%的新药通过了一项或多项加快开发和审评方法获得批准,FDA的高效审评机制为创新疗法快速进入市场开辟了绿色通道。
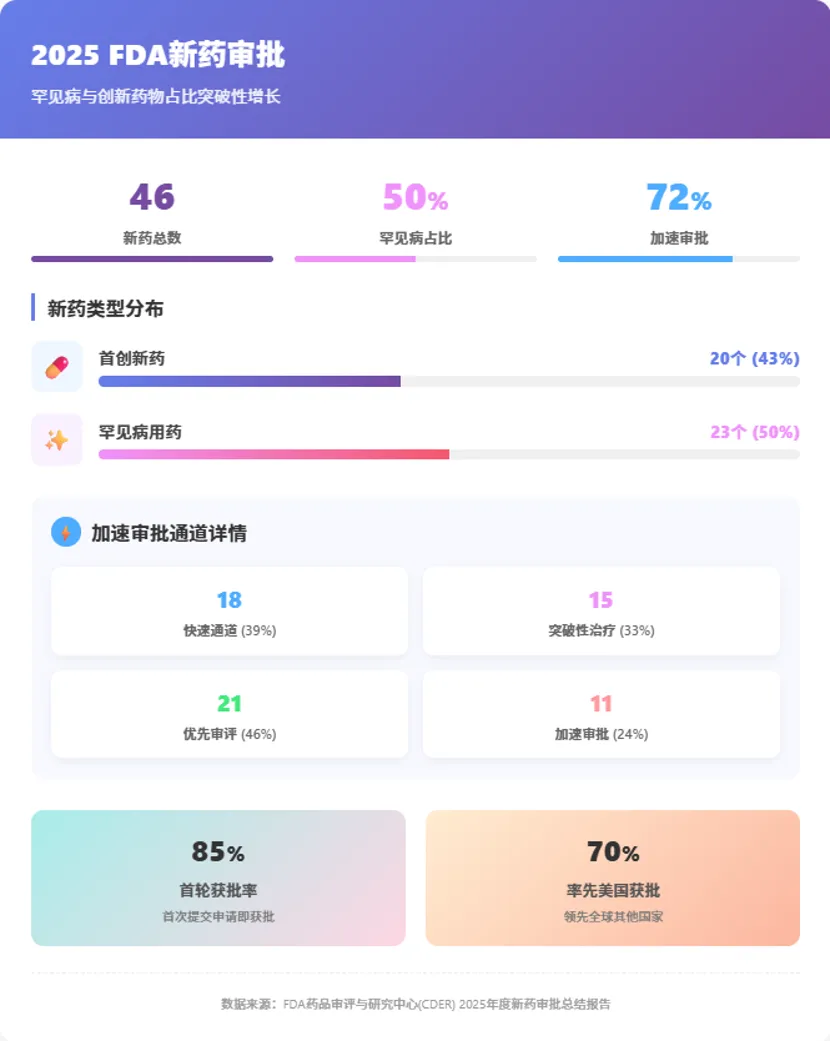
首创新药占比达43%
2025年,CDER共批准了46种新药,其中包括34种新分子实体和12种新型生物制剂。这一数字与近五年的平均水平持平,并高于自2007年以来的历史年均值(38种)。若算上生物制品评价与研究中心(CBER)的审批,全年共有58项新药获批。
其中最引人注目的是首创新药的涌现:在46种新药中,有20种(43%)被认定为具有全新作用机制的药物,例如:Journavx(suzetrigine)——首款非阿片类镇痛药,用于中重度疼痛;Tryptyr(acoltremon)——首款用于干眼症的全新机制药物;Blujepa(gepotidacin)——用于治疗特定尿路感染,后续还获批用于无并发症的泌尿生殖道淋病,展现了“一药多适应症”的潜力。
罕见病治疗迎突破
在2025年获批的新药中,整整一半(23种)获得了“孤儿药”认定,用于治疗在美国患者人数少于20万的罕见疾病。这一比例凸显了FDA与医药行业对罕见病群体日益增强的关注。
多项“首次”填补了治疗空白:Forzinity(elamipretide)——首个获批用于治疗Barth综合征的药物,这是一种危及生命的线粒体疾病,影响心脏、肌肉与免疫系统;Kygevvi(doxectine/doxribtimine)——用于治疗胸苷激酶2缺乏症,一种罕见肌肉疾病;Jascayd(nerandomilast)——用于特发性肺纤维化,后亦获批用于进行性肺纤维化。
此外,多个罕见肿瘤也迎来新药,如针对低级别浆液性卵巢癌、弥漫性中线胶质瘤、特定突变型非小细胞肺癌等。这些审批不仅为患者带来生存希望,也激励着更多针对罕见病的研发投入。
高效流程惠及患者
在保障安全与有效性的前提下,FDA通过多项加急程序显著提升了审批效率。2025年,72%的新药(33/46)使用了至少一种加急程序,包括快速通道、突破性疗法、优先审评和加速批准。
值得关注的是,85%的新药在第一轮审评中即获批准,反映出申报资料质量与审评沟通效率的双重提升;70%的新药在美国先于其他国家获批,凸显美国在全球医药创新中的引领地位;96%的新药在《处方药用户费用法案》(PDUFA)目标日期前完成审评,体现出审批流程的可预测性与规范性。
此外,FDA完成了新的局长国家优先审评券(CNPV)计划的首次行动,批准AugmentinXR(阿莫西林-克拉维酸钾)缓释片的重新上市,该药物可用于治疗社区获得性肺炎和急性细菌性鼻窦炎,加强了药品供应链,同时帮助应对持续的抗生素短缺问题。
生物类似药
2025年,CDER批准了10个参照药的18个新生物类似药,其中包括针对3个新参照药的4个生物类似药。这些生物类似药中有一些被批准为可互换生物类似药,即可以在不需要处方医生干预的情况下,根据州法律在药房中替代参照药。包括:Merilog(insulin aspart-szj)注射剂,用于改善糖尿病患者的血糖控制(参照药:Novolog),为首个针对Novolog的生物类似药。Kirsty(insulinaspart-xjhz)注射剂,用于改善糖尿病患者的血糖控制(参照药:Novolog)为首个针对Novolog的可互换生物类似药。
Omlyclo(omalizumab-igec)注射剂,用于治疗中重度持续性哮喘、伴有鼻息肉的慢性鼻窦炎作为附加治疗、免疫球蛋白E介导的食物过敏,以及HI抗组胺药治疗后的慢性自发性荨麻疹(参照药:Xolair),为可互换生物类似药。
Poherdy(pertuzumab-dpzb)输注剂,用于治疗HER2阳性转移性、局部晚期、炎性及早期乳腺癌。根据适应症,Poherdy与曲妥珠单抗和多西他赛或化疗联合使用(参照药:Perjeta),为可互换生物类似药。

 产业资讯
产业资讯
 医药魔方Info
医药魔方Info  2026-05-04
2026-05-04
 138
138

 产业资讯
产业资讯
 药融圈
药融圈  2026-05-04
2026-05-04
 133
133

 产业资讯
产业资讯
 Medaverse
Medaverse  2026-05-04
2026-05-04
 135
135
 热门资讯
热门资讯