 产业资讯
产业资讯
 药渡
药渡  2026-02-28
2026-02-28
 842
842
近日,国内IL-4Rα抗体赛道迎来新进展。2月25日至26日,国家药品监督管理局药品审评中心官网先后公示,康方生物自主研发的曼多奇单抗与三生国健自主研发的SSGJ-611两款重组抗IL-4Rα人源化单抗注射液的新药上市申请相继获得受理,适应症均聚焦于中重度特应性皮炎。
这标志着继康诺亚司普奇拜单抗率先打破进口垄断后,国产IL-4Rα单抗正密集进入申报上市阶段,国内自免赛道竞争正式从“独家领跑”迈入“群雄逐鹿”新格局。
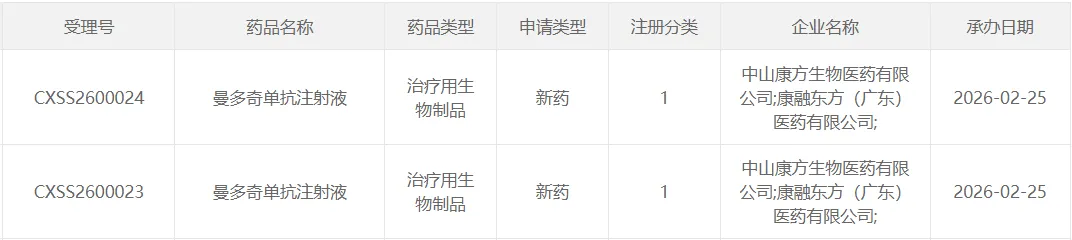
图1. 曼多奇单抗新药上市申请获受理,来源:CDE官网
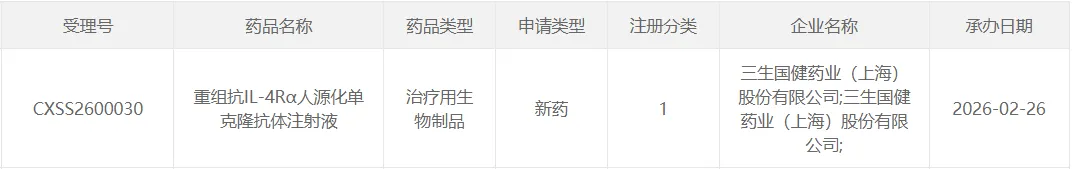
图2. SSGJ-611新药上市申请获受理,来源:CDE官网
PART.1
关于康方生物曼多奇单抗
康方生物的曼多奇单抗(AK120)是其进入上市申报阶段的第四款非肿瘤药物,此前PCSK9单抗伊努西单抗、IL-12/IL-23单抗依若奇单抗、IL-17A单抗古莫奇单抗已相继获批或申报上市,构建了覆盖心血管代谢、皮肤、关节等多领域的自免产品矩阵。
曼多奇单抗的申报基于关键注册性III期研究AK120-301的试验结果,该研究主要终点、关键次要终点及多项预设次要终点全部成功,展现出统计学显著性和临床意义的全面改善。
AK120-301研究显示,曼多奇单抗在显著改善患者皮损状态的同时,早期瘙痒改善疗效尤为突出,这一"快速止痒"特征对于特应性皮炎患者具有重要价值,因为剧烈瘙痒是导致睡眠障碍、焦虑抑郁及生活质量下降的核心症状。康方生物在申报成人适应症的同时,已前瞻性布局青少年特应性皮炎的关键III期研究,针对12-18岁这一对药物安全性要求更高的群体开发针对性方案,体现其全生命周期管理的战略意图。
更值得关注的是,康方生物并未止步于单抗产品,其升级迭代的IL-4R/ST2双抗AK139已进入II期临床,覆盖慢阻肺、重度哮喘、慢性自发性荨麻疹、过敏性鼻炎、慢性鼻窦炎伴鼻息肉、中重度特应性皮炎及结节性痒疹等多个适应症。这种"单抗打基础、双抗谋未来"的布局,旨在通过多靶点协同实现更广泛、更深入的2型炎症疾病控制,与度普利尤单抗的"Pipeline in a Drug"策略形成对标。
PART.2
关于三生国健SSGJ-611
三生国健作为中国大分子药物领域的先行者,其SSGJ-611的申报基于扎实的III期临床证据。该药物采用全新的人源化抗体可变区序列,对IL-4Rα靶点具有较高亲和力,在体外细胞实验中显示出与已上市同靶点抗体相当的生物活性。
其III期临床研究在中国成人中重度特应性皮炎患者中开展,采用600mg诱导剂量后300mg每两周维持(Q2W)的给药方案,在16周核心治疗期达到双主要终点:EASI-75(湿疹面积和严重程度指数改善≥75%)应答率与IGA 0/1(研究者整体评估评分0或1分且较基线改善≥2分)应答率均显著优于安慰剂组(P值均<0.0001)。
SSGJ-611的突出优势在于其长期疗效的稳定性。在52周维持治疗期,患者以300mg Q2W或300mg每四周(Q4W)给药,EASI-75维持率分别高达96.9%和95.8%,IGA 0/1维持率分别为89.6%和89.1%。这一数据展现出优于其他同靶点抗体试验设计的维持疗效趋势,意味着患者在接受诱导治疗后,可能以更低的给药频次维持长期疾病控制,显著提升治疗便利性与依从性。在瘙痒缓解方面,第16周瘙痒数值评定量表(NRS)周平均值较基线降低≥4分的应答率达45.4%,显著优于安慰剂组的15.6%(P<0.0001),快速止痒对于改善患者生活质量具有重要临床价值。
安全性方面,SSGJ-611在核心治疗期与长达52周的治疗期间均表现出良好的耐受性,未发现新的安全性信号。
PART.3
IL-4R赛道国内研发全景
当前中国IL-4Rα赛道已形成层次分明的竞争梯队,各企业基于自身资源禀赋与战略定位,探索差异化突破路径。
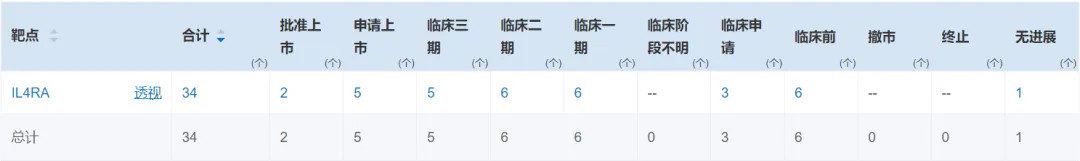
图3.
IL-4Rα赛道国内上市及在研药物数量,来源:药渡数据-全球药物库
第一梯队为已获批上市产品。康诺亚的司普奇拜单抗(Stapokibart)于2024年9月获批,成为国内首个、全球第二款IL-4Rα抗体,同年12月再获批慢性鼻窦炎伴鼻息肉适应症,2025年上半年销售额即达约1.7亿元,展现了国产替代的市场潜力。其成功纳入2025年医保目录,价格降幅超40%,医保支付价1039元/瓶(300mg),为度普利尤单抗(约1508元/支)的69%,初步建立了价格优势。
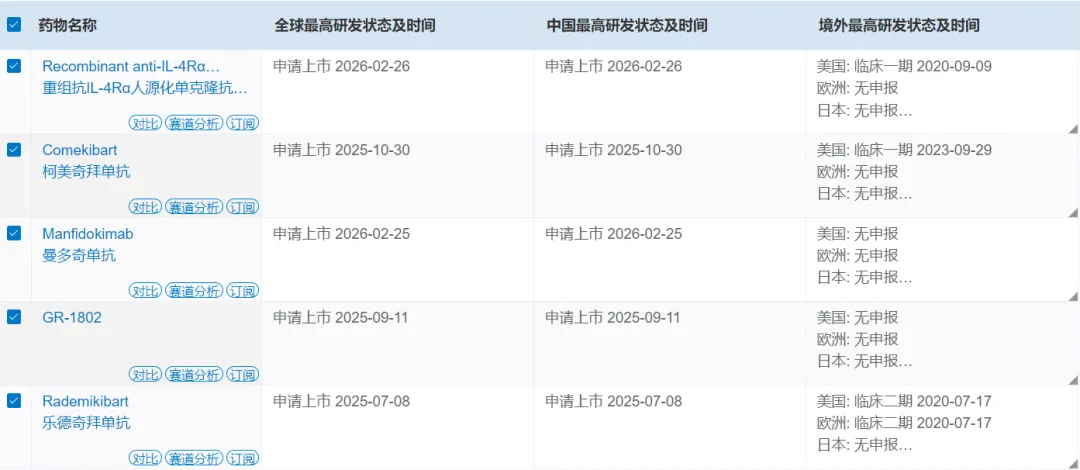
图4. IL-4Rα赛道国内已申报上市药物,来源:药渡数据-全球药物库
第二梯队为已申报上市的5款产品。除三生国健SSGJ-611与康方生物曼多奇单抗外,先声药业/康乃德的乐德奇拜单抗于2025年7月申报上市,其III期临床采用4周给药一次方案,直指患者依从性痛点;康哲药业/麦济生物的柯美奇拜单抗同样申报上市,宣称"全球首个长效IL-4R单抗",可实现每4周一次给药,一年仅需13次注射,较度普利尤单抗的26次直接减半;智翔金泰的泰利奇拜单抗于2025年9月申报上市,差异化布局六项适应症,包括慢性自发性荨麻疹这一度普利尤单抗尚未覆盖的领域,有望打破诺华奥马珠单抗的独家地位。
第三梯队为临床后期在研产品。恒瑞医药的SHR-1819针对结节性痒疹开展临床试验,该适应症目前仅度普利尤单抗获批,差异化突围意图明显;信达生物布局IL-4Rα/TSLP双抗,瞄准TSLP靶点在呼吸疾病中的关键作用;此外,石药集团、齐鲁制药等传统药企也在推进相关管线。
技术路线分化是本土突围的核心策略。长效化是主要方向,通过延长半衰期实现4周甚至8周给药,提升依从性;多靶点协同是升级路径,IL-4R/ST2、IL-4R/TSLP双抗旨在通过阻断多重炎症通路实现更优疗效;新剂型探索是创新前沿,恒瑞尝试开发可吸入给药的IL-4R抗体偶联糖皮质激素(自免ADC),若成功将彻底改变给药模式与安全性特征。
PART.4
度普利尤单抗的"危"与"机"
赛诺菲度普利尤单抗作为全球IL-4Rα领域的开创者与霸主,其该药2025年全年销售额达157.14亿欧元(约182.91亿美元),同比增长25.2%,近日再获批变应性真菌性鼻窦炎(AFRS)新适应症,累计获批适应症达11个,覆盖特应性皮炎、哮喘、慢性鼻窦炎伴鼻息肉、嗜酸性食管炎、结节性痒疹、慢性自发性荨麻疹、慢阻肺(COPD)等2型炎症疾病全谱系。其成功源于"Pipeline in a Drug"战略——以同一药物持续拓展适应症,积累跨疾病的临床证据与真实世界数据,构建难以复制的医学与商业护城河。
本土药企面临的挑战在于:其一,适应症广度差距显著,度普利尤单抗用8年时间建立的跨领域证据体系,后来者需以更高效的速度追赶;其二,临床验证的成熟度,度普利尤单抗在全球60多个国家的上市后经验与长期安全性数据,是新进入者短期内难以企及的;其三,价格天花板效应,2025年医保谈判后度普利尤单抗与司普奇拜单抗的价格已形成市场基准,后续产品若无法在疗效或给药便利性上实现突破性优势,价格博弈空间受限。
然而,机遇同样存在。中国特应性皮炎患者约7000万,中重度患者约1960万(2022年),预计2030年增至2280万,市场规模将从2024年的110亿元增长至2028年的297亿元,2033年达502亿元,年复合增长率28.1%。这一高速增长且远未饱和的市场,为本土产品提供了充分的放量空间。此外,青少年、儿童等特殊人群适应症,以及慢性自发性荨麻疹等度普利尤单抗尚未完全覆盖的领域,是差异化竞争的突破口。
结 语
三生国健SSGJ-611与康方生物曼多奇单抗的相继申报上市,标志着中国IL-4Rα赛道从"单点突破"进入"集群竞争"的新阶段。面对度普利尤单抗的全球霸主地位,本土创新药企以长效化、多靶点、差异化适应症为矛,以扎实的中国临床数据与快速商业化为盾,发起了集体突围。这场"诸神之战"的终局并非简单的"赢家通吃",而是通过充分竞争推动治疗标准升级、患者可及性提升与临床价值重构。
随着2026年多款国产产品有望密集获批上市,中国IL-4Rα市场将迎来真正的爆发期,而能够在这场战役中建立独特价值主张的企业,将不仅分享市场红利,更将参与全球2型炎症疾病治疗规则的制定,为中国创新药产业的崛起写下浓墨重彩的一笔。

 产业资讯
产业资讯
 医药魔方Info
医药魔方Info  2026-05-04
2026-05-04
 121
121

 产业资讯
产业资讯
 药融圈
药融圈  2026-05-04
2026-05-04
 118
118

 产业资讯
产业资讯
 Medaverse
Medaverse  2026-05-04
2026-05-04
 119
119
 热门资讯
热门资讯