 产业资讯
产业资讯
 生物世界
生物世界  2026-03-11
2026-03-11
 662
662

2017 年,美国FDA批准首款CD19自体CAR-T细胞疗法(Kymriah)上市,随后Yescarta等产品陆续获批,确立了基因工程改造的T细胞在血液肿瘤治疗中的临床价值。十余年间,自体CAR-T已在多种B细胞恶性肿瘤中完成关键注册性研究并实现商业化。
然而,自体CAR-T的个体化制造模式存在难以突破的瓶颈:需从患者体内采集 T 细胞,经体外激活、基因转导与扩增后回输,生产周期长达 2-4 周,且制造失败率高、成本居高不下,严重限制了其临床可及性。围绕“规模化生产与可及性提升”这一核心命题,CAR-T技术进入分化发展新阶段,异体通用型CAR-T与体内CAR-T成为两大核心探索方向。
所谓异体CAR-T,即使用健康供体细胞,经基因工程和基因编辑技术改造为现货通用型CAR-T细胞(UCAR-T),从根源上解决了自体CAR-T个性化、周期长、成本高、失败率高的痛点,具备即需即用、安全可控、成本可控的优势,成为CAR-T领域的重要发展方向。
2025 年以来,阿斯利康、艾伯维、BMS、礼来等国际制药巨头纷纷押注体内CAR-T(in vivo CAR-T)——这种无需体外复杂改造、直接在患者体内原位生成CAR-T细胞的技术,凭借“省时、低成本”的理论优势迅速成为行业热点。
事实上,自体CAR-T、UCAR-T、体内CAR-T并非“非此即彼”的替代关系,而是各有侧重、分层共存。自体CAR-T的工艺不断优化,成本逐步下降,短期内在血液瘤末线治疗等领域仍具有较大的不可替代性;而UCAR-T正通过持续技术迭代在特定赛道实现突围,正成为CAR-T领域不可或缺的重要发展方向,这一点从国内创新企业的探索成果中也可清晰窥见。自体CAR-T尚处技术研发的早期阶段,正如 20 年前的自体CAR-T或 10 年前的UCAR-T所处的开发阶段,仍有很大的需完善的空间,才能实现临床可及。
在此背景下,有必要对不同工程化路径的技术成熟度与临床阶段进行分层评估。
一、CAR-T 技术的路径分层:三大方向的差异化博弈
从工程实现方式与产业成熟度来看,当前CAR-T领域形成了三大清晰的技术路径,三者在优势、局限与临床阶段上差异显著,共同构成细胞治疗的多元发展格局,适配不同临床场景与患者需求。
1. 自体CAR-T:商业化成熟,但瓶颈凸显
作为目前最成熟的技术路径,自体CAR-T以“个体化定制”为核心,已在血液肿瘤领域完成充分商业验证,部分产品积累了 5 年以上长期生存数据,在实体瘤、自身免疫疾病领域也展现出潜在治疗价值。但其局限同样突出:生产周期长、成本高昂、批间差异大,且多次化疗后T细胞功能受损的患者,难以采集到高质量细胞用于制备,进一步限制了适用范围。
2. 体内CAR-T:热点赛道,但仍处早期探索
体内CAR-T的核心优势是“省去体外制造环节”,通过慢病毒、AAV等病毒载体或LNP等非病毒载体,将编码CAR的基因直接递送至患者体内原位生成CAR-T细胞,理论上可大幅降低治疗时间与成本,提升规模化可及性。
但该路径技术挑战严峻:体内递送效率与细胞特异性不足,可能导致CAR异常表达引发不良反应;CAR表达强度难以精准控制,影响治疗效果;病毒载体存在致癌风险,LNP载体可能引发肝脏毒性;更重要的是,目前整体仍处于早期临床探索阶段,长期疗效与持久性数据严重不足,落地仍需漫长技术攻坚。
3. UCAR-T:技术迭代,筑牢核心竞争力
作为异体CAR-T的核心形态,UCAR-T采用健康供体 T 细胞,经基因工程与基因编辑技术改造为“现货通用型”产品,可提前批量制备、冷冻储存,患者就诊后即需即用,从根源上解决了自体CAR-T的核心痛点,具备天然优势。
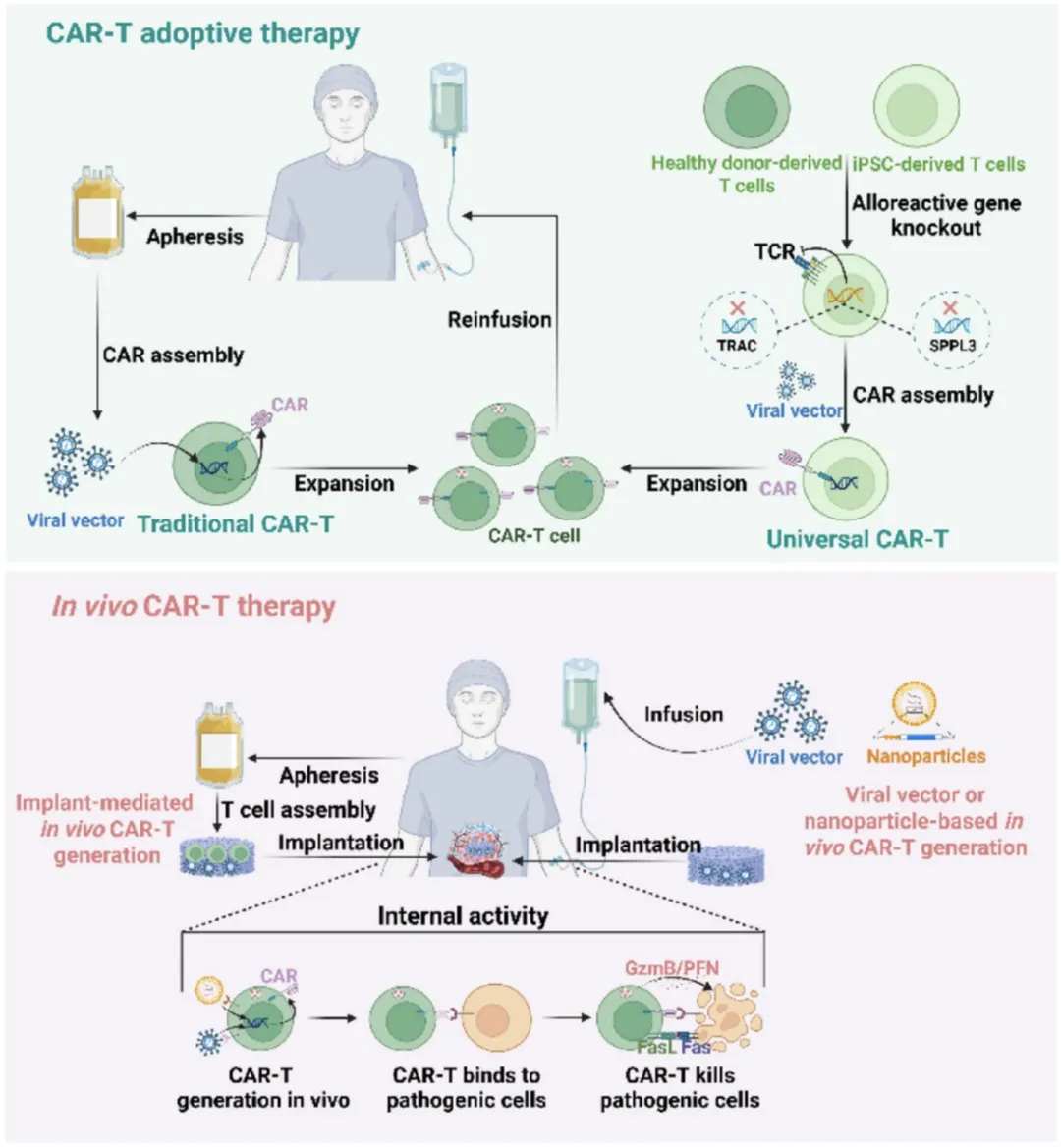
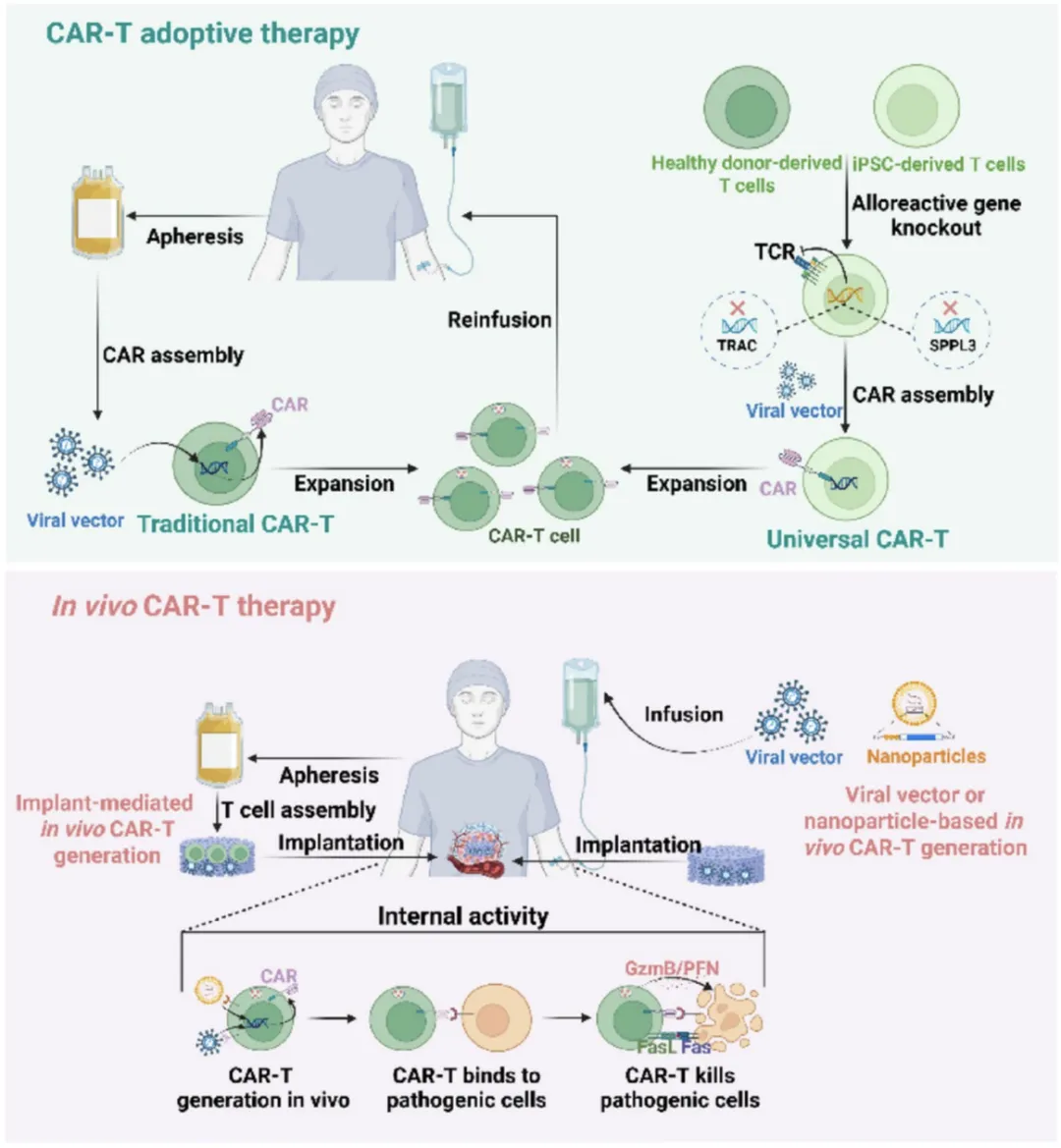
自体CAR-T、UCAR-T、体内CAR-T的技术路径
早期UCAR-T曾面临异体排斥、NK细胞介导的清除、体内存续时间短等技术难题,限制了临床应用。但随着CRISPR-Cas9等基因编辑技术的突破,这些瓶颈正被逐步打破,UCAR-T已从“被动逃逸”进入“主动防御”的技术升级新阶段,成为衔接自体CAR-T成熟性与体内CAR-T前瞻性的关键路径,临床价值正逐步得到验证。
二、UCAR-T的技术迭代:从“被动逃逸”到“主动防御”
早期UCAR-T的核心思路的是通过敲除TCR与B2M分子,降低移植物抗宿主病(GvHD)及宿主T细胞介导的排斥,但NK细胞对HLA-缺失细胞的清除问题,始终限制其体内存续时间与治疗效果,这也是早期UCAR-T面临的核心痛点,制约了其临床转化进程。基于B2M敲除的免疫逃逸策略,已被多项国内外临床实验证实疗效极其有限、开发难度极高,这或许是以该技术策略为分析蓝本的相关人士对UCAR-T缺乏信心的重要原因之一。
UCAR-T要想在提升体内持续性方面取得实质性突破,必须在抗排异新策略的探索上实现突破,事实上,目前已有不少科研与企业团队加速攻关,且取得了不俗的临床突破。
近年来,全球UCAR-T技术迎来迭代爆发,核心方向聚焦于“免疫调控”,通过多重基因编辑优化实现战略转变,多家企业的创新探索已进入临床验证阶段:
——“伪装术”:Caribo公司在敲除TCR和B2M的同时,敲入编码B2M-HLA-E融合蛋白的基因,双重削弱患者T细胞与NK细胞对UCAR-T细胞的排斥,延长体内存续时间;
——“反杀术”:科济生物通过装载抗NKG2A CAR,让UCAR-T细胞遭遇NK细胞时实现“反戈一击”,提升治疗持久性;
——“增强术”:敲除TGFBR2可有效抵抗T细胞耗竭;而国内邦耀生物实现进一步突破,在敲除PD-1的同时过表达PD-L1,从代谢调控与免疫抑制双维度优化UCAR-T细胞功能。
尤为值得关注的是,策略性敲除HLA分子的技术创新,成为破解UCAR-T免疫排斥难题的关键——该技术可让UCAR-T细胞在逃逸异体 T 细胞杀伤的同时,从根源上避免NK细胞活化,双维度解决异体细胞排斥问题。在这一核心技术路线的探索中,邦耀生物自主研发的策略性敲除HLA分子相关技术,成功实现了UCAR-T细胞在体内的高效存续与功能发挥,成为国产UCAR-T技术升级的重要参考。
三、赛道突围:自免领域成UCAR-T核心主场
血液肿瘤领域,自体CAR-T已实现商业化,市场趋于红海,UCAR-T单纯比拼疗效难以形成差异化优势。而自身免疫疾病领域仍是未充分开发的蓝海,且UCAR-T技术与之有着天生适配性:
一是患者自身T细胞质量差,系统性红斑狼疮、硬皮病等自身免疫疾病患者,T细胞功能本就紊乱,难以采集高质量自体T细胞制备CAR-T;
二是UCAR-T的现货属性可提前制备、冷冻储存,患者无需等待即可获得治疗,为治疗争取宝贵时间。
国内企业已率先抢跑:邦耀生物、启函生物、华夏英泰、先博生物等均已将各自UCAR-T疗法推进至自身免疫疾病的IIT或IND阶段。
自身免疫疾病领域,正在成为UCAR-T技术证明其临床价值的第一个关键战场。
四、UCAR-T的核心壁垒:安全性与清淋优化
自身免疫疾病患者免疫功能紊乱,对治疗耐受性更低,CAR-T细胞回输前的清淋强度与长期免疫恢复情况,成为评估UCAR-T成熟度的核心指标,也是其相较于体内CAR-T的重要优势。
传统UCAR-T治疗需依赖强效化疗清淋,这为患者带来感染、粒细胞缺乏等额外健康风险。如今,降低清淋强度甚至实现“零清淋”,成为UCAR-T技术升级的重要方向:
国外企业Allogene公司在早期临床试验发生严重不良事件后,已停用了相关的清淋抗体,新的技术设计(例如 Dagger 技术)正致力于降低对清淋的依赖;Fate公司更是宣称,通过多重基因编辑和多重基因工程修饰,有望实现“零清淋”。
国内企业探索同样走在前列,以邦耀生物的BRL-303 UCAR-T为例,其通过首创的多重基因编辑策略,在解决传统异体CAR-T排异问题的同时,也突破了对高强度清淋的依赖,其在临床安全性与耐受性上树立了行业新标杆。
更值得关注的是,UCAR-T的长期安全性优于体内CAR-T:体内CAR-T的病毒载体存在致癌风险、LNP载体存在肝脏毒性,长期安全性需大量数据积累;而UCAR-T是体外精准编辑、严格质控的“成品药”,每一批次都经过全面安全性检测,长期安全性数据更扎实、更可控,这也是其在自免领域的核心竞争力之一。
五、分层共存而非替代:UCAR-T的价值重构与未来展望
自体CAR-T、UCAR-T、体内CAR-T是基于技术成熟度、临床需求的分层共存格局:自体CAR-T聚焦肿瘤精准治疗,适配病情稳定、可等待制备周期的患者;UCAR-T重点突破可及性与标准化,在自身免疫疾病领域展现不可替代价值,适配病情紧急、无法采集高质量自体T细胞的患者;体内CAR-T代表长期创新方向,但落地仍需突破诸多瓶颈,短期内难以替代现有路径。
2026 年将成为UCAR-T临床价值验证的关键一年:Cellectis、Allogene、Caribou等国际企业计划公布相关临床数据,相关国内企业也将进一步披露UCAR-T在自身免疫疾病领域的进展。这些数据将让市场对UCAR-T的风险-收益比形成清晰认知,推动行业进入“数据驱动”新阶段。
CAR-T技术竞争的核心,是在不同疾病场景中实现安全性、持久性与可及性的平衡。体内CAR-T的热潮,不仅没有淘汰UCAR-T,反而推动其加速技术迭代、明确赛道定位——UCAR-T的价值,不在于取代自体CAR-T,而在于在可预见的临床阶段内,提供一种风险-收益结构更清晰、可及性更高的工程化解决方案,与其他路径互补,共同推动细胞治疗产业发展。
结语
CAR-产业正从“技术验证”向“平台分化”过渡,体内工程化与体外工程化路径,分别代表不同的实现逻辑与时间维度。在这一过程中,对技术成熟度的冷静评估与数据驱动判断,比简单的路线之争更具现实意义。
UCAR-T的价值,或许并不在于取代自体CAR-T,而在于在可预见的临床阶段内,提供一个风险—收益结构相对清晰的工程化解决方案。随着技术持续优化与临床数据积累,UCAR-T必将在细胞治疗领域占据重要地位,同时相信国内创新企业,也将凭借扎实的技术与临床积累,引领这一赛道走向更广阔的未来,让细胞治疗真正惠及更多患者。

 产业资讯
产业资讯
 医药魔方Info
医药魔方Info  2026-05-04
2026-05-04
 103
103

 产业资讯
产业资讯
 药融圈
药融圈  2026-05-04
2026-05-04
 99
99

 产业资讯
产业资讯
 Medaverse
Medaverse  2026-05-04
2026-05-04
 99
99
 热门资讯
热门资讯