 产业资讯
产业资讯
 生物制药小编
生物制药小编  2026-03-13
2026-03-13
 591
591
近日,Capricor Therapeutics公司宣布,FDA已撤销先前向其发出的完整回复函(CRL),正式恢复对Deramiocel治疗杜氏肌营养不良(DMD)相关的心肌病的生物制品许可申请(BLA)审查,预计将在2026年8月22日做出批准决定。
对于FDA来说,采取这种撤销CRL的行动是较为少见的,因为CRL通常意味着“该新药申请审查周期”已经完成,而申请人想要取得批准,需要重新提交申请,进入新一轮的审查周期。而在收到CRL后,Capricor快速、有效地对进行了回应,通过提供强有力的Ⅲ期临床数据(HOPE-3),成功说服FDA恢复审查并确定新的PDUFA日期。
如果这次审批顺利,Deramiocel将是首款获批上市的外泌体疗法,也是该类疾病的首款疗法,获得批准后,Capricor还将有资格获得一张优先审评券。
首个外泌体疗法
Deramiocel(CAP-1002)是一种同种异体外泌体细胞疗法,被开发用于治疗杜氏肌营养不良症(DMD)和贝克尔型肌营养不良症(BMD)等罕见神经肌肉疾病,尤其针对这类疾病进展导致的心肌病和骨骼肌功能恶化。
Deramiocel由心脏来源细胞(CDCs)组成,其主要通过分泌外泌体发挥治疗作用,这些外泌体能够靶向巨噬细胞,改变其表达谱,使其采用愈合表型而非促炎表型,进而实现免疫调节、抗纤维化和促进组织再生等作用。
先前,Deramiocel已获得孤儿药、再生医学先进疗法、先进治疗药品、罕见儿科疾病等多项重要监管认定。
Capricor最早于2024年10月向FDA提交了Deramiocel的BLA,用于治疗杜氏肌营养不良症(DMD)相关的心肌病。
但是在2025年7月,这一BLA申请遭到了FDA的拒批准,公司收到了完整回应函(CRL),在CRL中,FDA认为其提交的BLA缺乏足够的有效性证据,需补充更多临床数据才能证明其疗效,此外,Deramiocel的CMC也存在部分未解决的缺陷。
对CRL的迅速响应
对于该封CRL,Capricor的响应也是非常迅速的。2025年9月,在FDA公开CRL后,Capricor在其官网发布了对CRL的回应,表示十分有信心能够快速满足FDA提出的额外临床数据的要求。
这一响应主要得益于“有一项Deramiocel的Ⅲ期临床试验HOPE-3顶线数据”将要读出,以应对FDA提出的补充更多临床数据的要求。
2025年12月,Capricor报告了HOPE-3的顶线数据,试验结果显示:与安慰剂相比,HOPE-3达到了主要终点(PUL v2.0)和关键次要心脏终点(LVEF)目标,均达到统计学显著性。
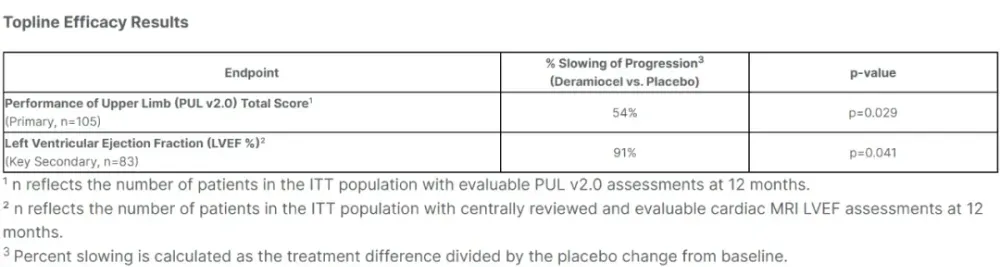
具体而言,与安慰剂相比,Deramiocel使上肢功能恶化速度(PUL
v2.0)减缓54%,心脏功能恶化速度(LVEF)减缓91%,所有第一类错误控制的次要终点均实现了统计学显著性。此外,HOPE-3结果显示其在骨骼和心脏方面具有临床意义和统计学显著的益处,Deramiocel的安全性和耐受性与既往临床研究一致。
这一临床数据令公司信心大增,Capricor认为,HOPE-3的数据进一步支持了Deramiocel作为治疗杜氏心肌病首选疗法的潜力,受此利好影响,Capricor股价应声这一临床数据发布后暴涨371%
同时,Capricor也认为HOPE-3的临床数据足以作为对CRL的回应,随后Capricor便向FDA提交了HOPE-3的关键数据,而且也获得了FDA的认可。在审查这些数据后,FDA在2026年1月正式要求提交完整的HOPE-3临床研究报告(CSR)及支持材料,且未提出开展额外的临床试验或新增患者数据的要求。
目前,在给公司的回复中,FDA尚未指出任何潜在的审查问题,这预示着此次Deramiocel成功获批的概率极大。

 产业资讯
产业资讯
 医药魔方Info
医药魔方Info  2026-05-04
2026-05-04
 103
103

 产业资讯
产业资讯
 药融圈
药融圈  2026-05-04
2026-05-04
 99
99

 产业资讯
产业资讯
 Medaverse
Medaverse  2026-05-04
2026-05-04
 99
99
 热门资讯
热门资讯