 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2026-03-25
2026-03-25
 2051
2051
3 月 24 日,信达生物宣布,其依莫芙普-α 注射液(IBI302)在中国新生血管性年龄相关性黄斑变性(nAMD)人群中开展的 III 期临床研究(STAR,登记号:NCT05972473)达成 52 周主要终点。

来源:信达生物官微
在此研究中,依莫芙普-α 视力改善效果非劣效于阿柏西普,同时展现了 16 周超长间隔给药的临床优势以及降低 MA(黄斑萎缩)发生的潜力。这是国内首个自主研发的眼底新药抗 VEGF 融合蛋白药物在首个 III 期研究里实现 16 周给药间隔的能力。
依莫芙普-α 是信达生物自主研发的一种全球首创双特异性重组全人源融合蛋白。N 端为 VEGF 结合域,能够与 VEGF 家族结合阻断 VEGF 介导的信号通路,抑制血管内皮细胞的生存、增殖,从而抑制血管新生,降低血管渗透性,减少血管渗漏;C 端为补体结合域,能够通过特异性结合 C3b 和 C4b,抑制补体经典途径和旁路途经的激活,减轻补体活化介导的炎症反应。
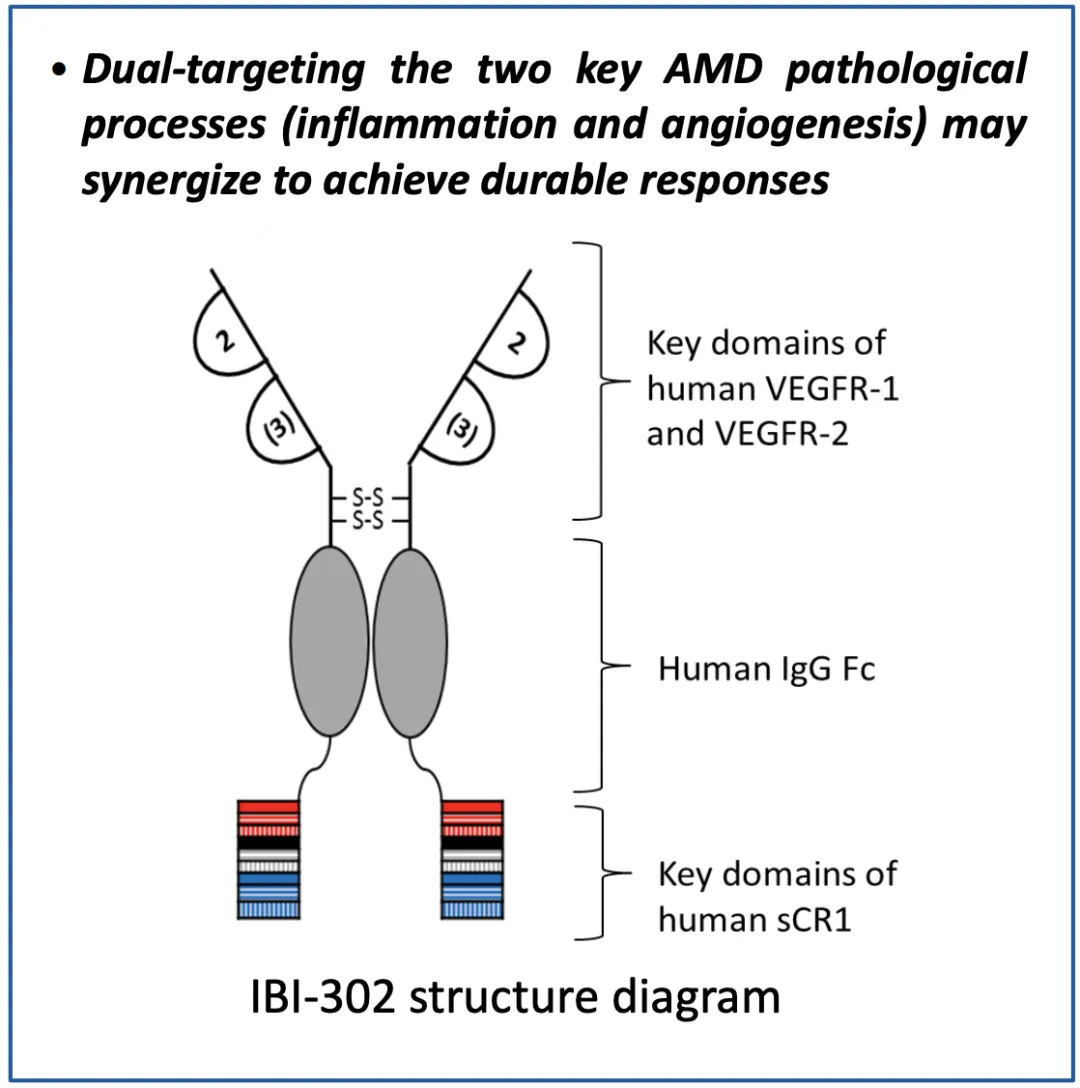
来源:信达生物
STAR 是一项在中国 nAMD 受试者中评估 8mg IBI302 疗效和安全性的 III 期临床研究。600 例受试者以 1:1 随机分配至 8mg IBI302 组及 2mg 阿柏西普组。IBI302 组和 2mg 阿柏西普组均接受每 4 周一次,共三次负荷治疗。完成负荷治疗后,IBI302 组根据第 16 和 20 周疾病活动情况个性化调整给药间隔,按照 Q8W、Q12W 或 Q16W 间隔完成后续治疗,2mg 阿柏西普组按照 Q8W 间隔完成后续治疗。
该研究持续 100 周,主要终点为:第 44、48 和 52 周时,研究眼最佳矫正视力(BCVA)字母数均值较基线的改变。本研究随机分层因素为:研究眼光学相干断层扫描(OCT)上是否含有 II 型脉络膜新生血管(CNV),以及研究眼既往是否接受过抗 VEGF 治疗。
研究共入组 600 例受试者,基线平均 BCVA 为 58.1 个 ETDRS 字母,基线平均中央视网膜厚度(CST)为 420.75 μm。基线时,研究眼既往未接受过抗 VEGF 治疗的比例约 65%。
结果显示:8mg IBI302 组视力改善非劣效于 2mg 阿柏西普组,研究主要终点达成。第 44、48 和 52 周时,8mg IBI302 和 2mg 阿柏西普组平均 BCVA 较基线变化最小二乘估计均值(SE)分别为 10.37(0.547)和 10.11(0.545)个 ETDRS 字母。
给药间隔延长:8mg IBI302 组中,约 86% 受试者可实现≥Q12W 的给药间隔,72.8% 受试者可以达到 Q16W 给药。至第 52 周时,约 95% 接受 Q12/16W 给药的受试者可以维持此给药间隔而无需接受再治疗。此外,56.3% 的受试者在 W24 无疾病活动,具备延长至 Q20W 给药的潜力。
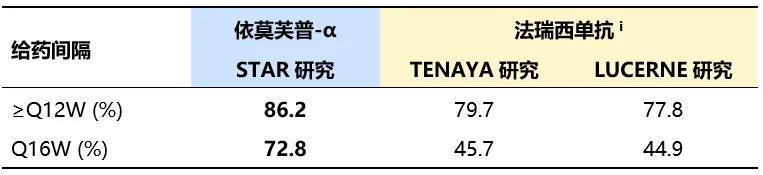
来源:信达生物官微
解剖学疗效指标改善:两组受试者第 16 周时黄斑中心凹无视网膜内积液且无视网膜下积液的比例相近,第 52 周时包括 CST 较基线变化等各解剖学指标较基线改善程度相近。
抗黄斑萎缩(MA)趋势:第 52 周时,8mg IBI302 组和 2mg 阿柏西普组新发 MA 的比例分别为 1.5% 和 2.9%,IBI302 治疗后新发 MA 比例相较阿柏西普组下降约 50%,趋势与 II 期研究结果一致,提示 IBI302 具有减少 MA 发生的潜力。
安全性良好:8mg IBI302 组总体不良事件发生率与阿柏西普 2mg 组相当。眼部不良事件以轻中度为主,观察或常规处理后预后良好。
基于以上研究结果,信达生物正积极准备递交新药上市申请。

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-05-18
2026-05-18
 345
345

 研发追踪
研发追踪
 医药魔方Info
医药魔方Info  2026-05-18
2026-05-18
 410
410

 研发追踪
研发追踪
 药研网
药研网  2026-05-18
2026-05-18
 326
326
 热门资讯
热门资讯