 研发追踪
研发追踪
 医药魔方Info
医药魔方Info  2026-05-04
2026-05-04
 15
15
4月27日,Intellia Therapeutics宣布Lonvo-z(NTLA-2002)治疗遗传性血管性水肿(HAE)的全球III期HAELO研究取得了积极结果。该公司计划向FDA提交滚动BLA申请,预计在2026年下半年完成申请工作,期待在2027年上半年在美国商业化Lonvo-z。

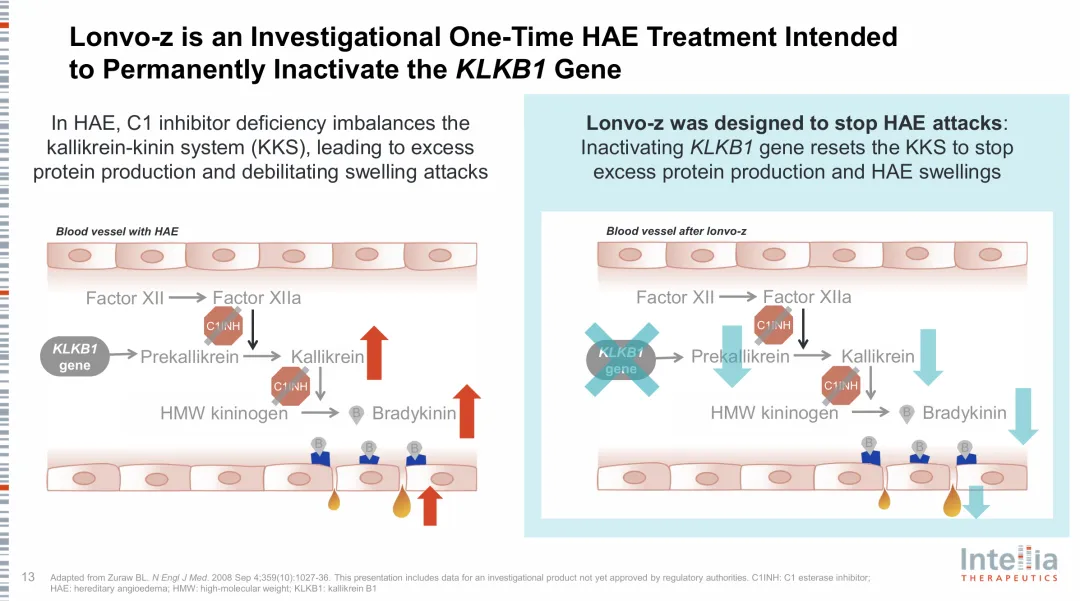
Lonvo-z是Intellia
Therapeutics基于CRISPR/Cas9技术开发的一款体内基因编辑疗法,旨在通过敲除KLKB1基因来减少激肽释放酶原(PKK)及激肽释放酶的产生,进而降低与HAE发病相关的缓激肽水平,最终实现疾病治愈效果。该药物有潜力成为全球首个通过一次注射即可实现功能性治愈HAE的药物。
Lonvo-z于2021年进入临床阶段,其疗效已在II期研究中初步显现。数据显示,治疗16周后,接受25mg和50mg剂量治疗的HAE患者,每月HAE发作次数均为0.70,安慰剂组这一数字为2.8。此外,40%(4/10)和73%(8/11)的患者在接受25mg和50mg剂量治疗的16周内疾病未发作且无需再接受治疗。
本次III期HAELO研究顺利完成进一步验证了Lonvo-z的治疗潜力。该研究纳入了80例I型或II型HAE患者,评估了Lonvo-z(50mg)的疗效和安全性。
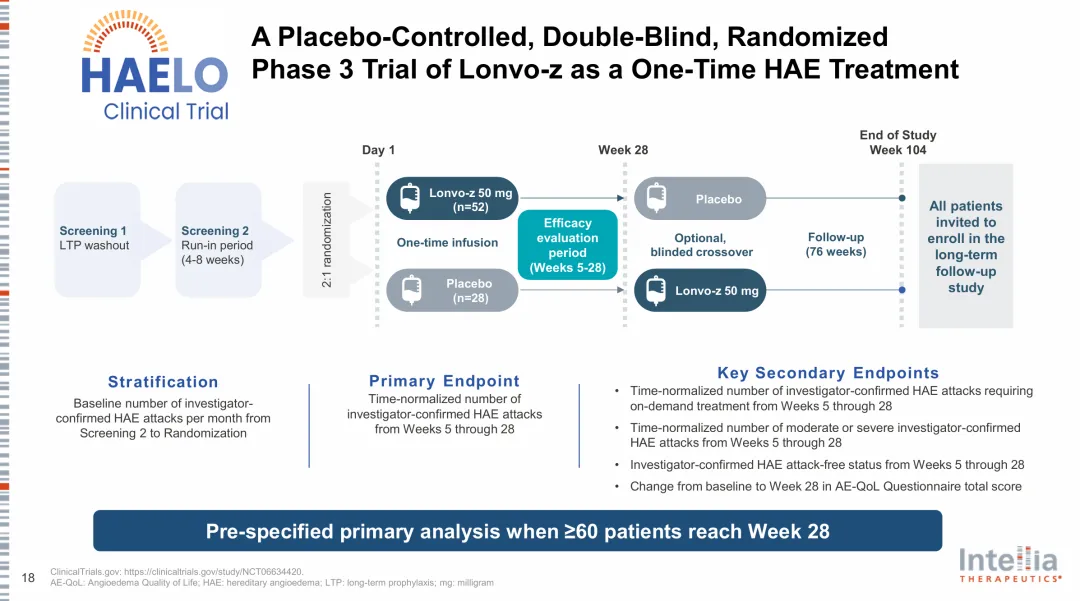
结果显示,该研究达到了主要终点。在六个月的疗效评估期(第5-28周)内,Lonvo-z组患者的HAE发作频率相比安慰剂组降低了87%(平均月发作率:0.26
vs 2.10,p<0.0001)。
此外,该研究达到了所有关键次要终点。其中包括62%的患者在六个月疗效评估期内疾病未发作且无需再接受治疗,而安慰剂组这一比例为11%。
值得一提的是,在基线或第28周后交叉接受Lonvo-z治疗的患者均无需接受长期预防治疗。
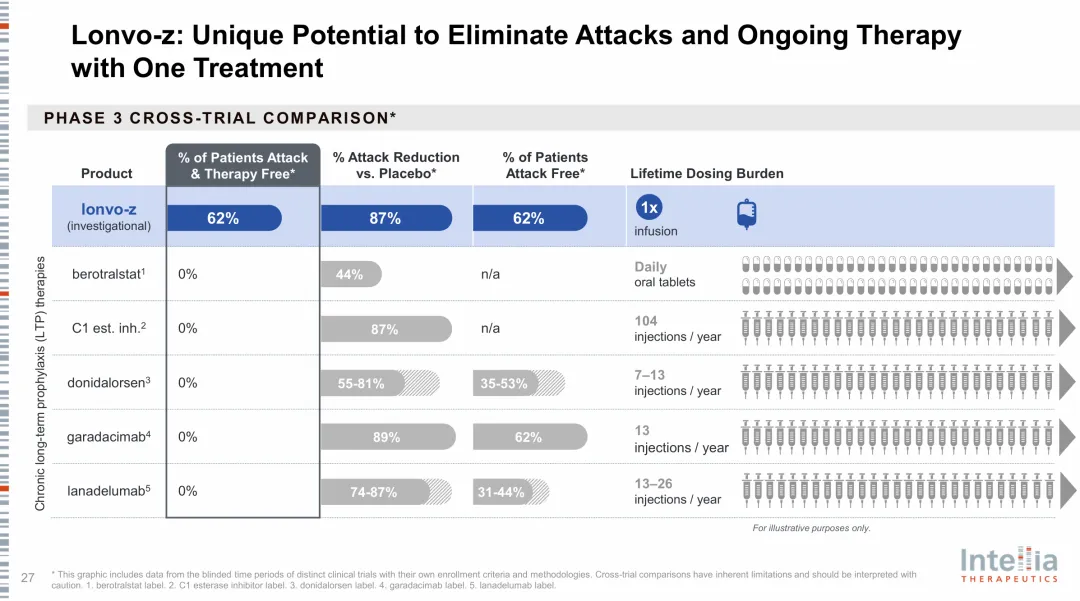
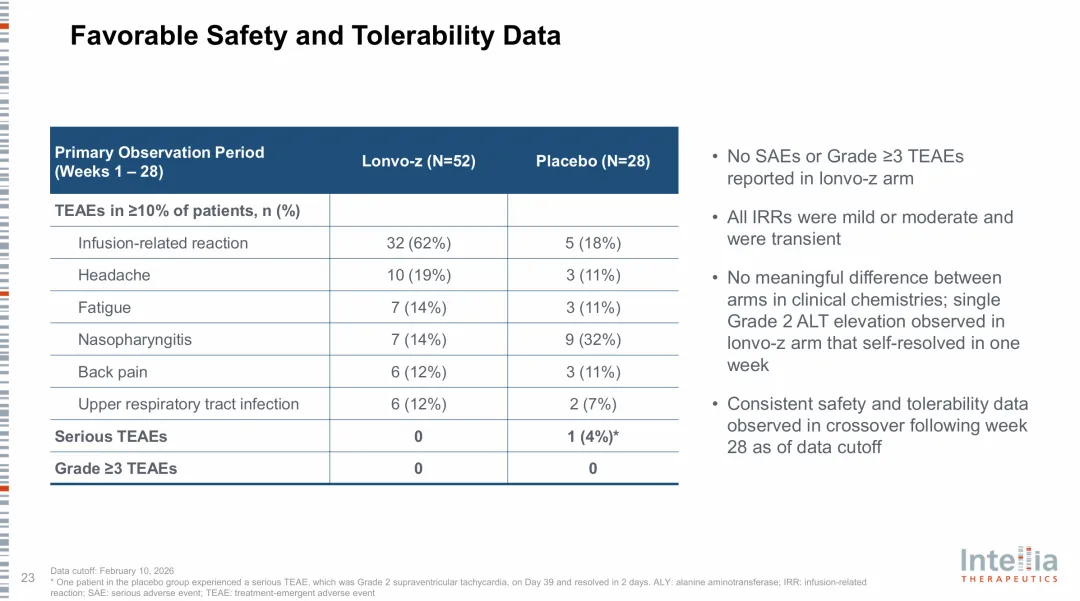
在该研究中,Lonvo-z具有良好的安全性和耐受性。在观察初期(输注日至第28周),最常见的治疗期间不良事件(TEAEs)为输注相关反应、头痛、疲劳、鼻咽炎、背痛、上呼吸道感染。截至2026年2月10日,所有TEAEs均为轻度或中度,未观察到严重不良事件。
HAE是一种罕见的遗传性疾病,患者因缓激肽水平过高,面部、上呼吸道、腹部和四肢等多个身体部位反复出现可能危及生命的肿胀(血管性水肿)。
据估计,每5万人中就有1人患有HAE。这类患者可以接受预防性治疗或者按需治疗来管理疾病。目前的治疗方案均为终身治疗,给药频率高达每周注射两次或每日口服一次。但这些治疗方案仍然无法避免疾病复发。
原文链接:

 研发追踪
研发追踪
 医药时间
医药时间  2026-05-04
2026-05-04
 13
13

 研发追踪
研发追踪
 药讯随说
药讯随说  2026-05-04
2026-05-04
 13
13

 研发追踪
研发追踪
 医药笔记
医药笔记  2026-05-04
2026-05-04
 13
13
 热门资讯
热门资讯