 产业资讯
产业资讯
 药智数据
药智数据  2026-05-13
2026-05-13
 21
21
01
临床试验类型分布情况
2026年4月,据药智数据企业版【中国临床试验】数据库显示CDE公示登记的药物临床试验共计493个临床试验登记。其中,化学药物临床试验以359项占据主要,生物制品和中药则分别为123项和11项。
在试验分期方面,占比最大的是“其他”临床试验,达到了38.9%,总计192项试验,且这些试验中化学药物的生物等效性试验占绝大多数。其次是“1期”试验,合计136项研究,另外2期和3期试验数量分别为70、60项,4期临床试验仅有5项。
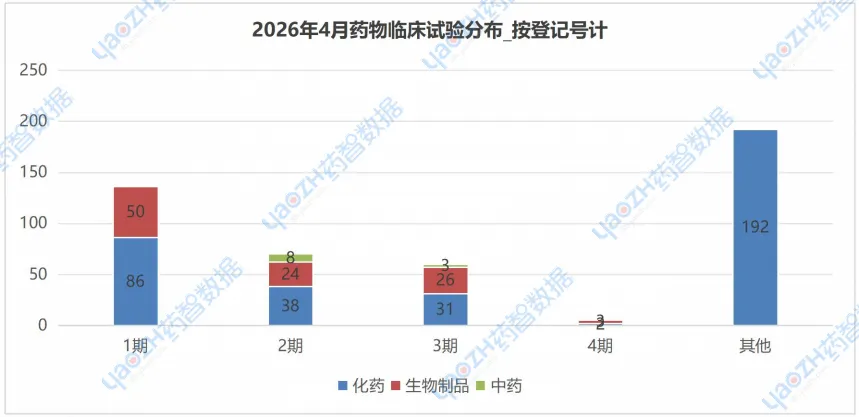
注:由于存在同一临床试验属于多个临床分期的情况,所以上述统计数量会多于临床试验总数
02
药物临床试验品种分析
在2026年4月CDE登记的药物临床试验品种top10榜单中,“非奈利酮片”以14个登记试验位列榜首,且都为生物等效性临床试验。“非奈利酮片”的14个临床试验分别由烟台鲁银药业有限公司、成都天台山制药股份有限公司、浙江华义制药有限公司、扬子江药业集团有限公司等公司申办,针对的临床试验适应症都为“与2型糖尿病相关的慢性肾脏病成人患者(伴白蛋白尿),以降低肾小球滤过率估计值(eGFR)持续下降、终末期肾病、心血管死亡和因心力衰竭住院的风险”。“苯磺酸美洛加巴林片”以8个临床试验位列第二,均为生物等效性临床试验。
更多详细信息,请详见下图或访问药智数据企业版【中国临床试验】数据库进行查询。
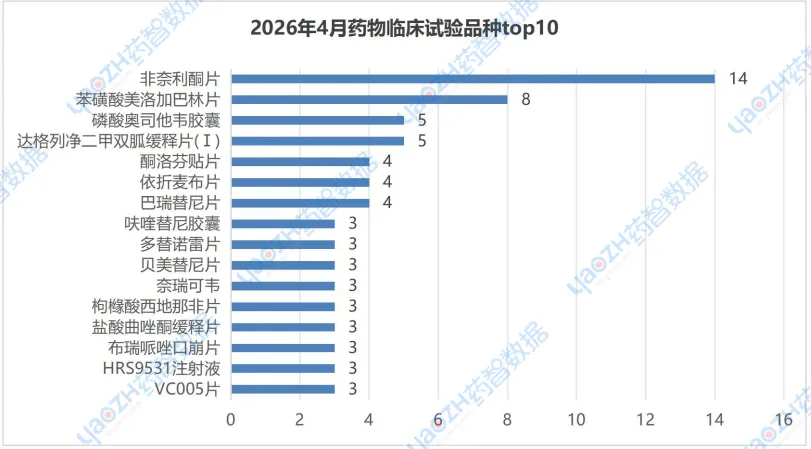
注:由于存在并列情况,所以上述排行可能不止10个
03
药物临床试验申报单位分析
在2026年4月的CDE药物临床试验申办单位排行榜中,“齐鲁制药有限公司”以7个临床登记试验位列榜首,“齐鲁制药有限公司”的7项试验涵盖了6个不同品种的临床试验,既有新药临床试验,也有生物等效性试验,具体为“非奈利酮片、QLG1091、QLS1410片、QLS5212、单唾液酸四己糖神经节苷脂钠注射液”等;“辰欣药业股份有限公司”以6个临床登记试验位列第二,且6个临床登记试验全部为生物等效性试验。
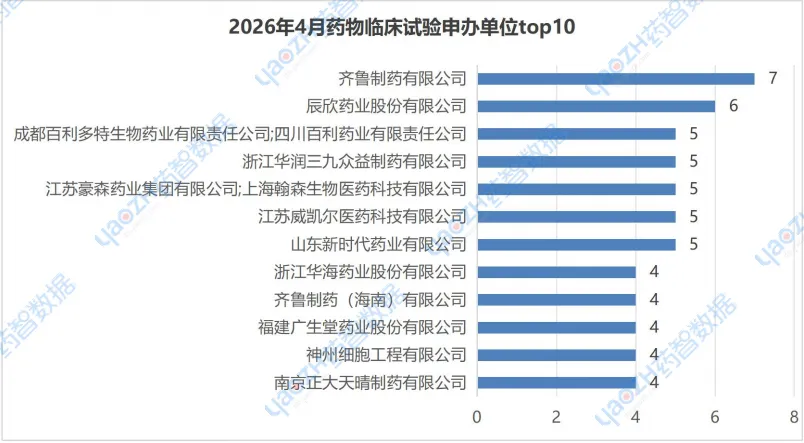
注:由于存在并列情况,所以上述排行可能不止10个
04
药物临床试验机构分析
在2026年4月的CDE药物临床试验登记公示中,“河南中汇心血管病医院”以牵头16个临床试验位列榜首,且这16个临床试验全部为生物等效性试验。
“北京大学肿瘤医院”则以牵头14个临床试验位列第二,且均为新药临床试验。更多详细信息,请详见下图或访问药智数据企业版【中国临床试验】数据库进行查询。
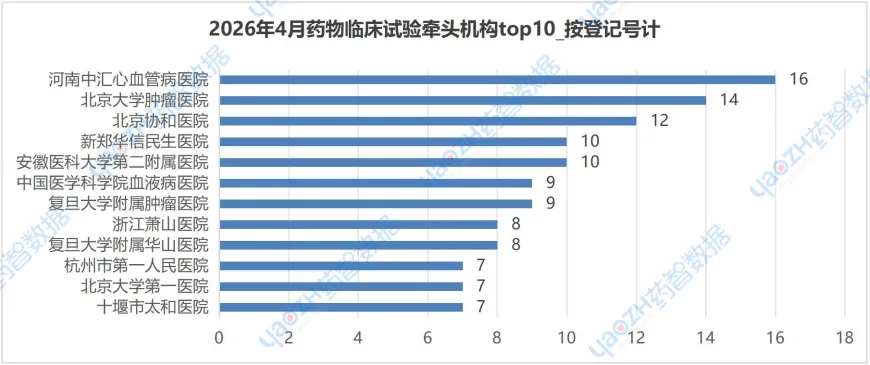
注:由于存在并列情况,所以上述排行可能不止10个
05
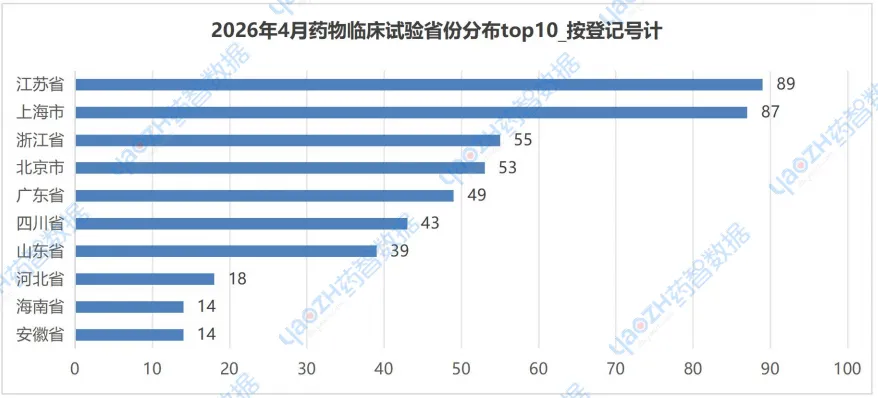
临床试验省份分布情况
在2026年4月的CDE药物临床试验登记公示中,按申办单位所在地区统计,临床试验省份分布见下图,江苏以89个临床试验登记位居首位,上海和浙江位列第二和第三。更多详细信息,请详见下图或访问药智数据企业版【中国临床试验】数据库进行查询。
06
临床试验关键事件
4月1日,荣昌生物自主研发的靶向PSMA和B7H3的双抗ADC药物RC288获NMPA批准开展I/Ⅱa期临床试验,用于治疗晚期实体肿瘤,这是首个进入临床阶段的双抗ADC。
同期,百济神州注射用BG-C0979获批临床,用于治疗晚期实体瘤。该药靶向ADAM9,是继RC288后国内第二款获批临床的ADAM9 ADC。
4月13日,3期RASolute 302临床试验公布积极结果。口服RAS(ON)多选择性抑制剂Daraxonrasib(RMC-6236)用于经治的转移性胰腺癌患者,相比标准化疗,中位总生存期从6.7个月提升至13.2个月,死亡风险降低60%。
4月15日,靶向HER2的口服抗癌药塞伐艾替尼在中国获批,用于二线治疗HER2突变非小细胞肺癌。
4月10日,全球首款DLL3/CD3双抗塔拉妥单抗在国内获批上市,用于三线治疗小细胞肺癌。
创新药上市申请:4月,共有5款1类创新生物制品提交上市申请,创单月历史纪录,其中包括先声药业的IL-4Rα单抗乐德奇拜单抗等。

 产业资讯
产业资讯
 CHC医疗传媒
CHC医疗传媒  2026-05-13
2026-05-13
 24
24

 产业资讯
产业资讯
 建国路128号
建国路128号  2026-05-13
2026-05-13
 23
23

 产业资讯
产业资讯
 药创新
药创新  2026-05-13
2026-05-13
 21
21
 热门资讯
热门资讯