 会员动态
会员动态
 医药笔记
医药笔记  2025-08-26
2025-08-26
 1990
1990
2025年8月25日,信达生物宣布PD-1/IL-2抗体融合蛋白获得美国FDA批准,开展治疗鳞状非小细胞肺癌首个全球关键三期临床研究。


IBI363引领了肿瘤免疫赛道细胞因子领域的研发进展,分子设计上进行了独特的差异化设计,IL-2保留了对IL-2Rα的亲和力,减弱了IL-2Rβγ的活性,通过对肿瘤组织CD8
T细胞的激活,与PD-1抗体发挥协同抗肿瘤活性,同时有效的控制了毒副作用。
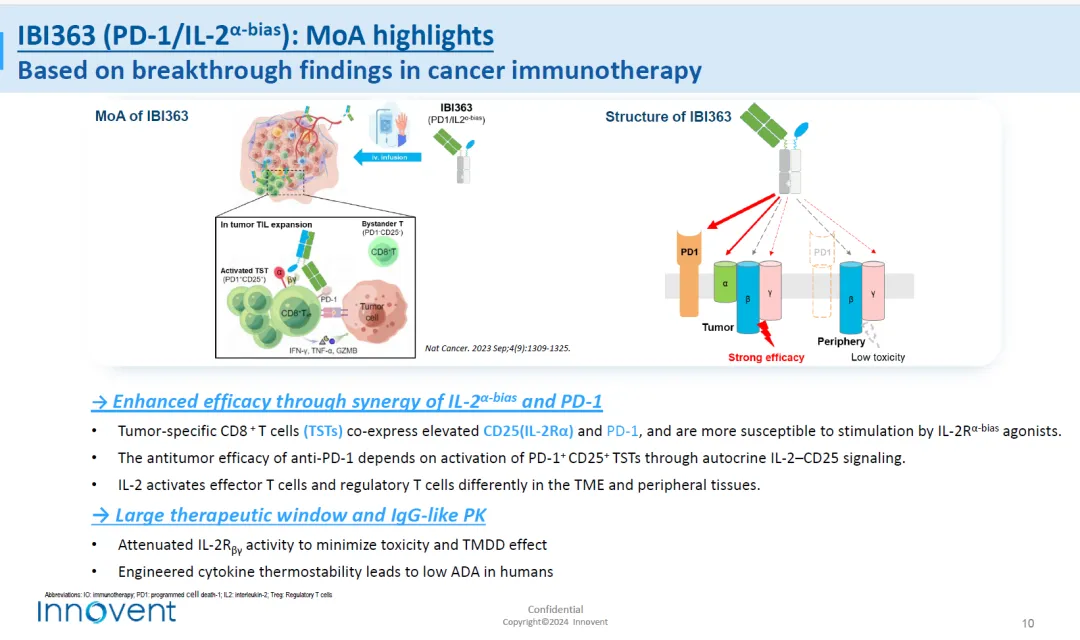
IBI363在国内已经拿下两项适应症突破疗法认证,包括PD-1及含铂化疗后线治疗鳞状非小细胞肺癌,一线治疗晚期黑色素瘤。IBI363在美国鳞状非小细胞肺癌适应症获得快速通道资格。


总结
信达生物围绕肿瘤这一核心治疗领域,通过新一代IO疗法+新一代ADC实现迭代布局。新一代IO疗法的核心即为PD-1/IL-2抗体融合蛋白IBI363,新一代ADC包括双靶点ADC、双毒素ADC等。此次IBI363获批开展鳞状非小细胞肺癌全球三期临床,标志着国际化再加速,也标志着这一创新双免疫疗法的全球开发进入最后的POC阶段。

 会员动态
会员动态
 维健医药
维健医药  2026-04-27
2026-04-27
 355
355

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-27
2026-04-27
 355
355

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-20
2026-04-20
 529
529
 热门资讯
热门资讯