 研发追踪
研发追踪
 基因弧
基因弧  2026-03-16
2026-03-16
 1408
1408
导语
杜氏肌营养不良症 (Duchenne muscular dystrophy, DMD) 是一种由抗肌萎缩蛋白 (dystrophin) 编码基因突变引起的X染色体连锁的隐性遗传病。目前,与DMD基因相关的变异已超过7000个,绝大多数为外显子区域的缺失、重复和点突变。据统计,DMD男婴发病率约1/5000-1/3500,已纳入我国《第一批罕见病目录》。尽管目前多款DMD疗法已经取得了突破性进展,但其发病机制复杂且治疗方法存在疗效有限、成本较高等问题,亟需进一步的研究和创新。
近日,Regenxbio公司在2026年肌肉萎缩症协会 (MDA) 临床与科学会议上发布了其针对杜氏肌营养不良症 (DMD) 的在研AAV基因疗法RGX-202关键性临床试验AFFINITY DUCHENNE的积极中期数据。数据显示,这款潜在同类最佳 (best-in-class) 基因疗法在给药一年后不仅在运动功能和心脏健康方面展现出显著的稳定和改善作用,其安全性数据也异常亮眼。公司计划于2026年年中申请FDA的BLA前会议,确证性试验同步顺利推进,已进入商业化倒计时阶段。

▲ 来源:iStock
▉ 功能与心脏双重获益,改写疾病自然病程
当地时间2026年3月11日,Regenxbio公司 (Nasdaq:RGNX) 在3月8日至11日于奥兰多举行的2026年肌肉萎缩症协会 (MDA) 临床与科学会议上发布了其针对杜氏肌营养不良症 (DMD) 的在研AAV基因疗法RGX-202关键性临床试验AFFINITY DUCHENNE (NCT05693142) 的积极中期数据。公司计划于2026年年中申请FDA的BLA前会议,确证性试验同步顺利推进,已进入商业化倒计时阶段。

▲ 新闻稿截图
RGX-202是一款基于AAV8载体的潜在同类最佳 (best-in-class) 基因疗法,搭载肌肉特异性启动子Spc5-12,旨在递送表达微肌营养不良蛋白的转基因进入骨骼肌和心肌组织,改善杜氏肌营养不良症患者的肌肉功能和预后。
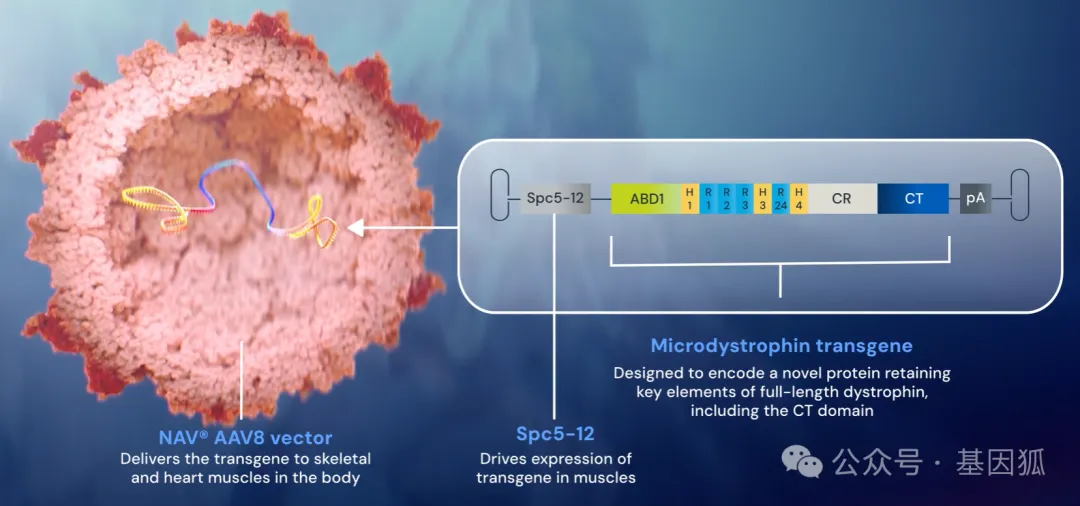
▲ RGX-202载体设计特点
RGX-202的独特之处在于编码的微抗肌萎缩蛋白中包含了关键的C末端 (CT) 结构域,可以产生功能更接近天然蛋白的微肌营养不良蛋白。研究表明,CT结构域对于招募各类蛋白复合物、维持肌膜 (sarcolemma) 稳定性具有重要的信号传导作用。在一例给药时仅3.6岁的患儿中,第12周的微抗肌萎缩蛋白表达量高达51.2%,远超10%的治疗阈值,充分证实了其密码子优化技术在提升蛋白翻译效率方面的成功。RGX-202是目前唯一进入后期临床开发阶段且包含CT结构域的DMD基因疗法。
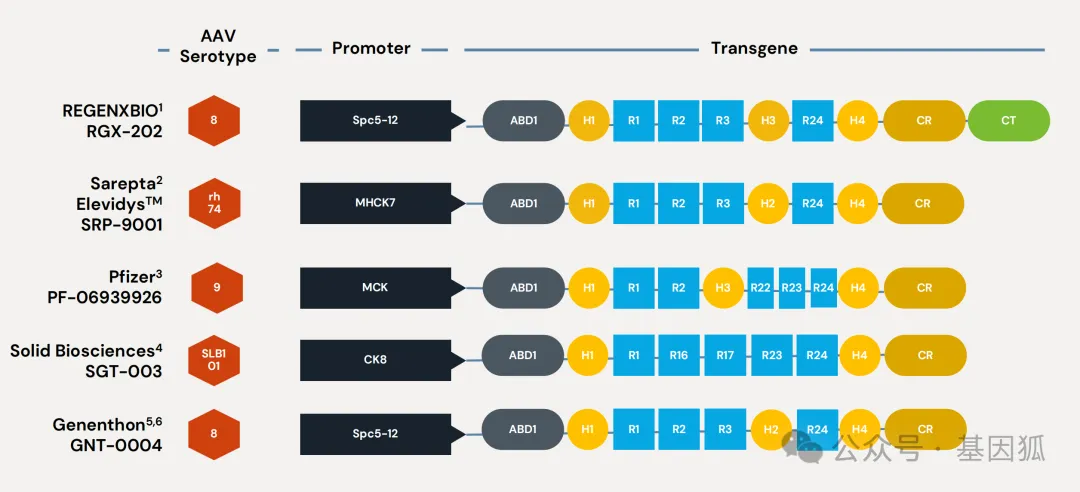
▲ RGX-202载体设计特点
AFFINITY DUCHENNE是一项多中心、开放标签 I/II/III期临床试验,共入组30名受试者,主要终点为治疗12周后,患者体内微肌营养不良蛋白表达量≥10%,次要终点包括4岁及以上受试者在定时功能测试中较基线的变化。该研究的设计也考虑到了对更低龄患者群体的评估。1至4岁受试者将使用皮博迪发育运动发育量表第三版 (PDMS-3) 和 SV95C进行评估。这体现了基因治疗向早期干预发展的趋势,旨在疾病对肌肉造成不可逆损伤之前进行治疗,从而最大程度地保留患者的运动功能,改善长期预后。

▲ AFFINITY DUCHENNE试验临床设计
此次AFFINITY DUCHENNE试验的关键剂量组 (2x10^14 GC/kg) 中,7名受试者(其中5名给药时已年满8岁或以上) 在治疗一年后,不仅成功阻止了疾病的恶化,反而实现了运动功能的逆转。数据显示,在北极星移动评价量表 (NSAA) 中,大龄受试者 (n=5) 与cTAP模型预测的自然疾病进展相比平均提升了5.2分。10米步行/跑步速度 (10MWR) 和攀爬时间等计时功能测试同样印证了这一功能获益。
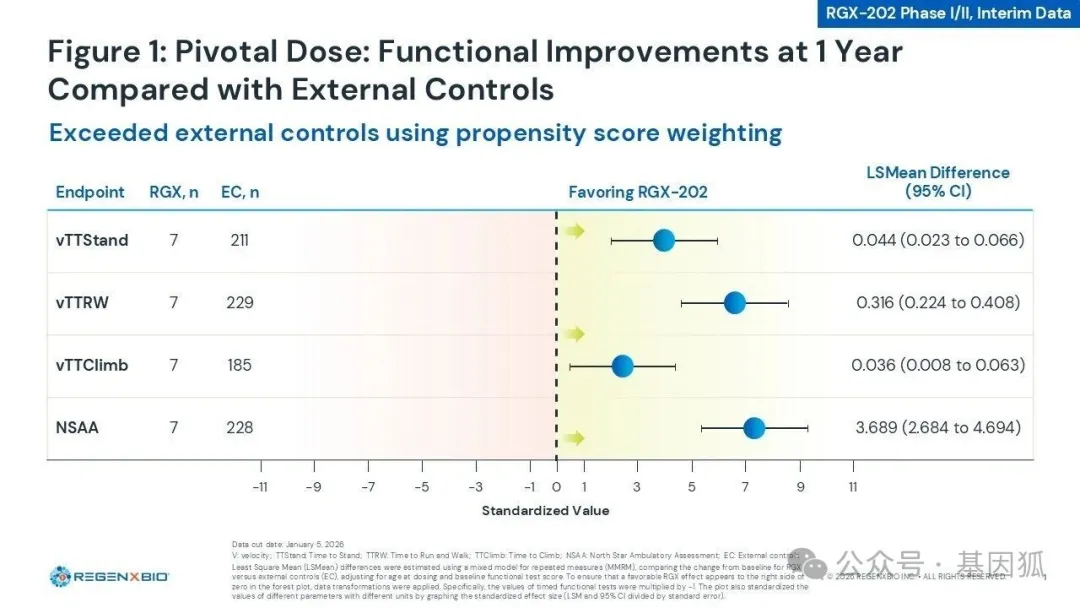
▲ RGX-202临床数据
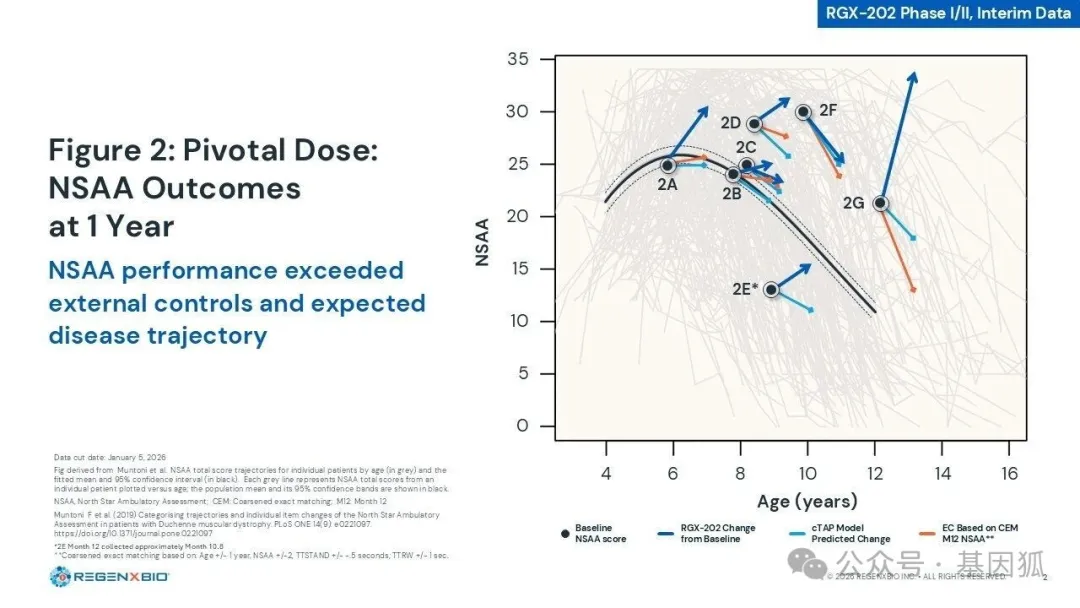
▲ RGX-202临床数据
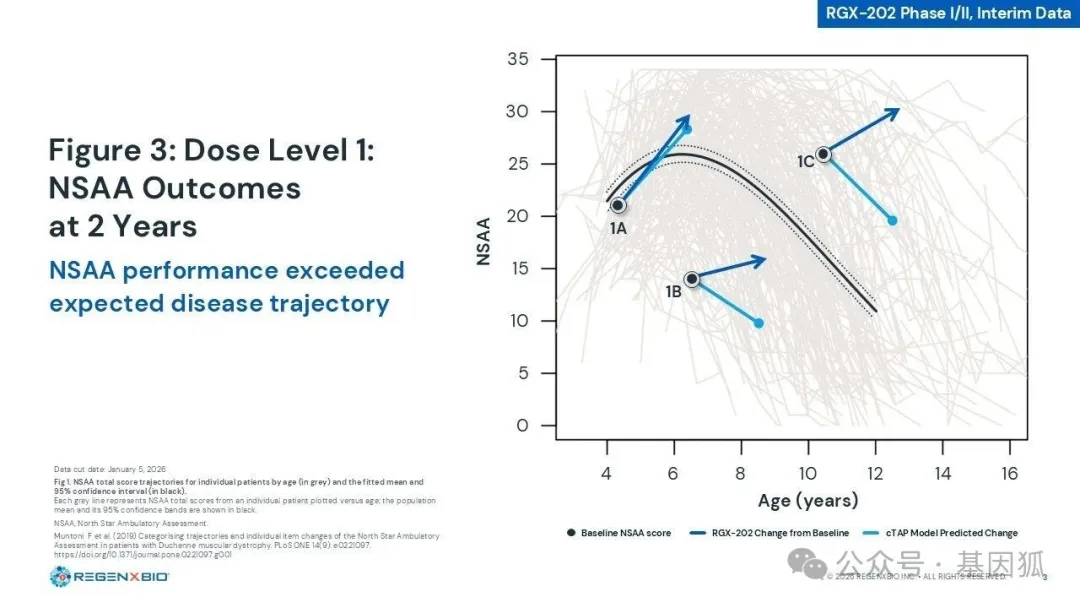
▲ RGX-202临床数据
与此同时,最新的心脏MRI数据显示,治疗后一年的患者在左心室射血分数 (平均维持在61.6%) 及整体圆周应变等核心指标上保持了极高的稳定性,这为DMD患者的长期生存质量提供了坚实的保障。
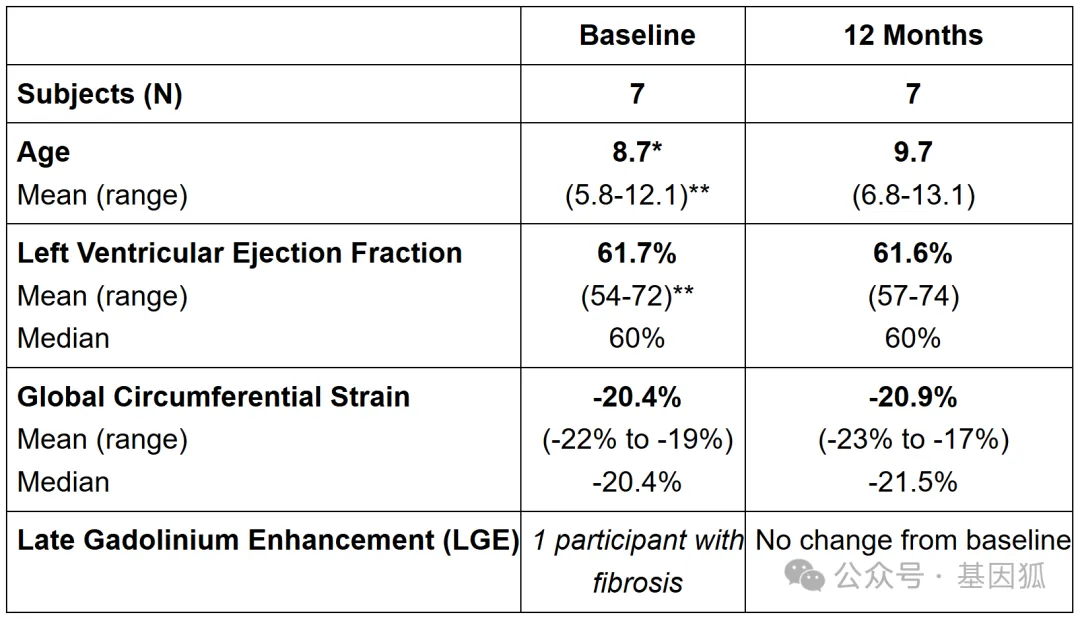
▲ RGX-202临床数据
▉ 安全性破局:突破基因疗法的肝毒性瓶颈
安全性方面,在长达两年的随访期内,所有1至<12岁的关键剂量患儿均未出现肝损伤迹象。代表DMD肝脏炎症的平均γ-谷氨酰转移酶 (GGT) 和总胆红素未超出正常上限。此外,肌酸激酶、ALT和AST水平的全面下降,进一步证实了RGX-202对肌肉细胞膜的保护作用。
截止2026年1月5日,RGX-202 在I/II期研究中耐受性良好,尚未报告严重不良事件 (SAEs) 或特别关注的不良事件 (AESIs)。常见的药物相关不良事件包括呕吐、疲乏和恶心。早期临床数据显示了强大的蛋白表达能力和明确的功能改善,同时安全性记录良好,为通过加速审批通道在2026年提交BLA铺平了道路。
值得一提的是,RGX-202的生产依托于公司专有的NAVXpress®悬浮细胞培养工艺,可以实现年产高达2500剂的生产能力。该平台不仅产量高,而且能够稳定生产出完整衣壳率超过80%的高纯度产品,极大降低了无效空衣壳引发的免疫风暴风险,这一指标在DMD基因疗法领域处于领先地位,构筑了公司强大的竞争壁垒。
DMD基因治疗赛道竞争异常激烈,目前市场上已有首款获批疗法 (Elevidys),但业界一直在寻找疗效更持久、安全性更高、尤其是能覆盖更大年龄段患儿的迭代方案。RGX-202的积极进展代表了DMD基因治疗正从“有或无”的1.0时代,迈向追求“更好功能”的2.0时代。如果关键性试验能够成功验证其分子设计的优越性,不仅将为DMD患者带来更优的治疗选择,也将为其他大片段基因相关疾病的基因替代疗法设计提供宝贵的科学范例,推动整个基因治疗领域向更精准、更高效的方向发展。
原链接:

 研发追踪
研发追踪
 医药时间
医药时间  2026-05-04
2026-05-04
 517
517

 研发追踪
研发追踪
 药讯随说
药讯随说  2026-05-04
2026-05-04
 518
518

 研发追踪
研发追踪
 医药笔记
医药笔记  2026-05-04
2026-05-04
 500
500
 热门资讯
热门资讯