 会员动态
会员动态
 UmabsDB
UmabsDB  2025-09-19
2025-09-19
 1720
1720
近期,根据UmabsDB数据库的记录,正大天晴在clinical trials网站上,登记了一项PD-1/TGF-β融合蛋白药物TQB2868 ,联合盐酸安罗替尼、吉西他滨和紫杉醇,与安慰剂联合吉西他滨和紫杉醇对比,在一线治疗转移性胰腺导管腺癌 (mPDAC)受试者中,启动了一项3期临床试验NCT07165951,这也是该款产品首次进入三期临床。

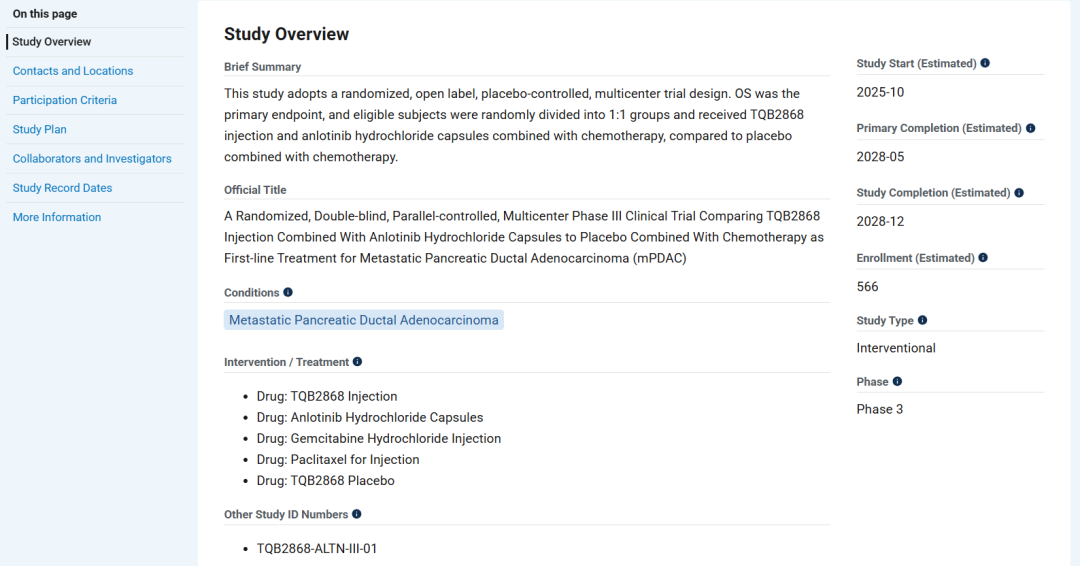
本次三期临床的主要终点为OS,计划入组566例患者,同样由复旦大学附属肿瘤医院的虞先濬博士担任主要研究者,其之前已经担任三项胰腺癌ADC药物三期临床的主要研究者(胰腺癌:乐普TF
ADC启动首个三期临床)。
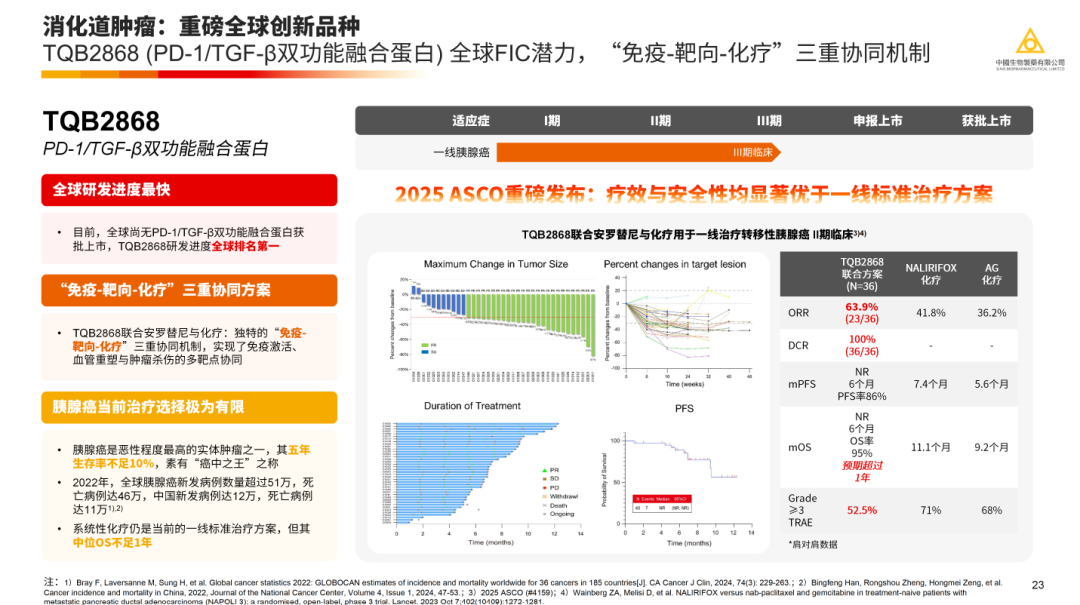
TQB2868为正大天晴自主研发的PD-1/TGF-β双功能分子,其具有“免疫-靶向-化疗”的三重机制。
2025年ASCO会议期间公布的联合盐酸安罗替尼及化疗在一线胰腺癌中二期临床结果,其响应率达到了63.9%,6个月OS达到95%,显著高于当前的一线标准疗法,同时三级以上TRAES为52.5%,也将提升当前疗法的耐受性。
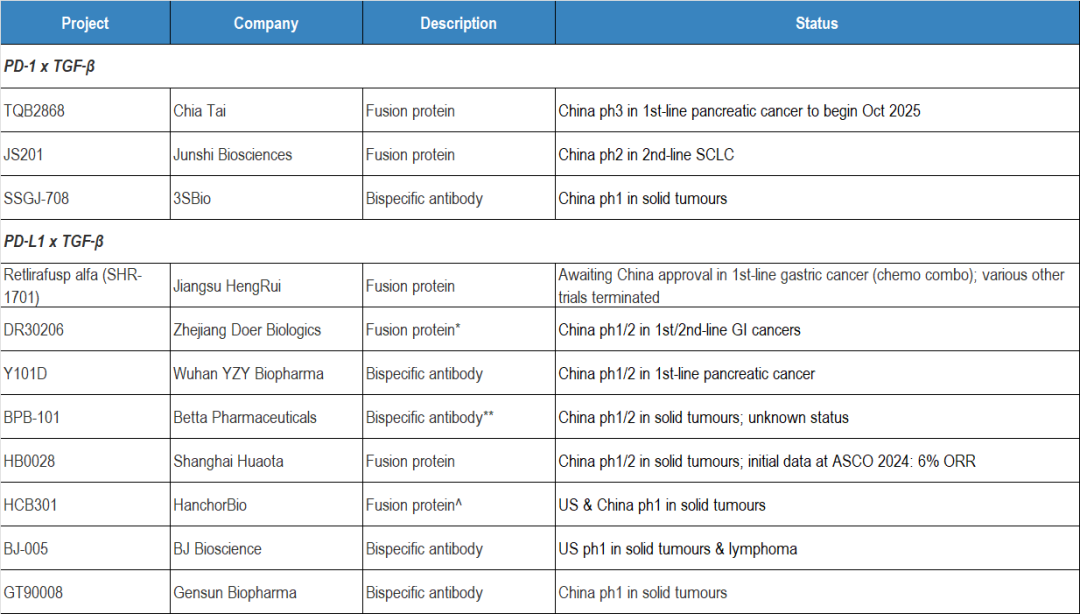
此前德国Merck开发的PD-L1/TGF-β融合蛋白 bintrafusp
alfa一度被寄予厚望,但是在包括非小细胞肺癌的多个临床中不及预期,已经停止研发。但是中国的多个快速跟进项目却并没用停止研发,反而在寻求新的适应症突破。
恒瑞的PD-L1/TGF-β融合蛋白瑞拉芙普-α(SHR-1701)已经递交了一线胃癌的上市申请(全球首款:恒瑞递交PD-L1/TGF-βRII双功能融合蛋白上市申请),正大天晴的PD-1/TGF-β融合蛋白药物TQB2868则在一线胰腺癌取得突破,君实的PD-1/TGF-β融合蛋白药物JS201则在小细胞肺癌进行二期临床探索。
同时近期胰腺癌相关的研究进展显著,信达生物的CLDN18.2 ADC药物IBI343、信诺维的TF ADC药物XNW28012和乐普生物的TF
ADC药物MRG004A,先后启动了系统治疗失败后的胰腺癌治疗三期临床(突破前夜:两款ADC启动胰腺癌三期临床试验),同时齐鲁制药则将相关疗法推进到CLND18.2阳性胰腺癌的一线治疗(全球首个:齐鲁CLDN18.2/CD3双抗启动胰腺癌三期临床)。
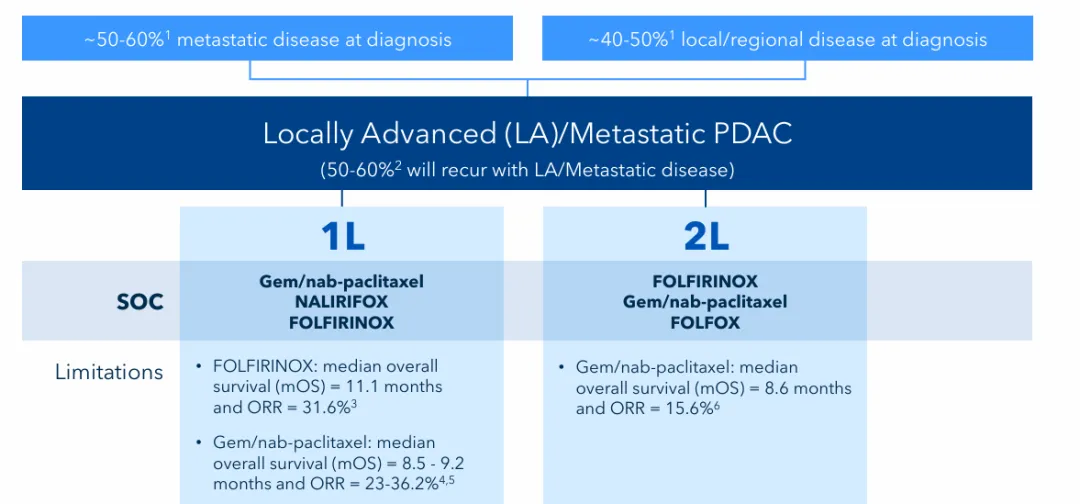
此前转移性胰腺癌的一线治疗,以奥沙利铂+伊立替康+氟尿嘧啶+亚叶酸钙的四联疗法为主,中位生存期为11.1个月,二线治疗为吉西他滨+白蛋白紫杉醇的联合疗法为主,中位生存期为8.6个月,期待相关疗法均能取得突破。

 会员动态
会员动态
 维健医药
维健医药  2026-04-27
2026-04-27
 301
301

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-27
2026-04-27
 298
298

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-20
2026-04-20
 489
489
 热门资讯
热门资讯