 会员动态
会员动态
 药物杂评
药物杂评  2025-09-23
2025-09-23
 2497
2497

最新消息,百利天恒EGFR/HER3双抗ADC药物BL-B01D1(伦康依隆妥单抗,iza-bren)尿路上皮癌将加冕该产品第七项中国突破性疗法适应症。
在此之前,BL-B01D1已获得中国突破性疗法药物的6个适应症是:鼻咽癌、非鳞状非小细胞肺癌、EGFR野生非小细胞肺癌、食管癌、小细胞肺癌及注射用BL-B01D1/iza-bren皮上卵巢癌、输卵管癌或原发生粘膜癌适应症。
此外,该药物用于治疗携带EGFR外显子19缺失或外显子21 L858R替换突变且既往接受过EGFR-TKI和含铂化疗治疗的局部晚期或转移性非小细胞肺癌,还获得了美国FDA的突破性疗法认定。
这大概率是中国创新药物纳入中国突破性疗法最多的药物了,不能说唯一,甚少在近一两年内极其罕见。
这款全球首创、新概念且唯一进入III期临床阶段的EGFR/HER3双抗药物ADC,正在中国和美国进行40多项针对多种肿瘤的临床研究。
2025年7月,百利天恒披露BL-B01D1治疗鼻咽癌III期临床达到主要终点,这是BL-B01D1首个达到终点的三期临床适应症,也是全球首个完成III期的双抗ADC药物。
BL-B01D1治疗鼻咽癌已向中国国家药监局递交了上市申请,由于其已获得突破性疗法认定,将获得优先审批流程。百利天恒董事长朱义上周在接受采访时表示,预测该药物在2026年上市。
据百利天恒2025年8月20日披露的半年报显示,BL-B01D1的非小细胞肺癌、小细胞肺癌、HR+HER2乳腺癌、三阴性乳腺癌、食管癌、胃癌、结直肠癌、胆道癌、头颈鳞癌、妇科肿瘤、泌尿系统肿瘤及其他实体瘤适应症,均已处于III期临床。
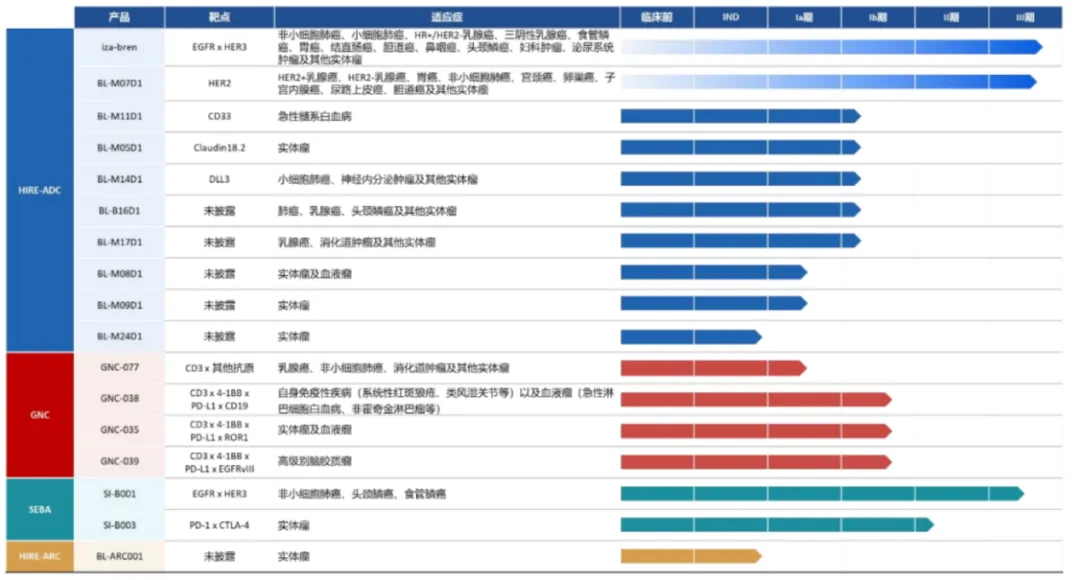
同时,BL-B01D1还在美国启动3项2/3期注册临床。
2023年12月,百利天恒与百时美施贵宝(BMS)达成一项全球战略合作协议,将BL-B01D1的海外开发和商业化权益授予BMS。这笔交易的首付款高达8亿美元,潜在总金额高达84亿美元。

除BL-B01D1外,百利天恒共有15款创新药处于临床试验阶段及2款创新药处于IND受理阶段,其中3款已进入Ⅲ期注册临床阶段。
在双抗药物上,百利天恒布局了EGFR/HER3双抗SI-B001,其针对PD1经治的EGFRwt NSCLC末线,目前已进入临床III期。ADC药物上,百利天恒布布局了 BL-M07D1,M11D1等6款新药,其中BL-B07D1针对HER2+乳腺癌的早期数据展现出BIC潜力,目前已进入临床III期。
朱义对外表示,百利天恒投资20亿在成都建设创新药的商业化供应基地——抗体生产第六期,他称新建产能达到70%就能创造100亿以上产值。
百利天恒是中国创新药最有创造力企业之一,市值仅次于百济神州、恒瑞医药的三强之一,市值1503亿元。

 会员动态
会员动态
 维健医药
维健医药  2026-04-27
2026-04-27
 301
301

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-27
2026-04-27
 298
298

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-20
2026-04-20
 489
489
 热门资讯
热门资讯