 会员动态
会员动态
 医药时间
医药时间  2025-11-27
2025-11-27
 980
980
11 月 26 日,CDE 官网显示,贝达药业盐酸恩沙替尼胶囊新适应症上市申请获受理。根据临床试验进展,丁香园 Insight 数据库推测适应症为:间变性淋巴瘤激酶(ALK)阳性的非小细胞肺癌(NSCLC)术后辅助治疗。这是国内首个寻求将适应症拓展至术后人群的 ALK 抑制剂。

来源:CDE 官网
2025 年 10 月,贝达药业在 ESMO 大会上以口头报告形式披露了恩沙替尼用于 IB-IIIB 期 ALK 阳性 NSCLC 术后辅助治疗的 III 期 ELEVATE 研究数据。
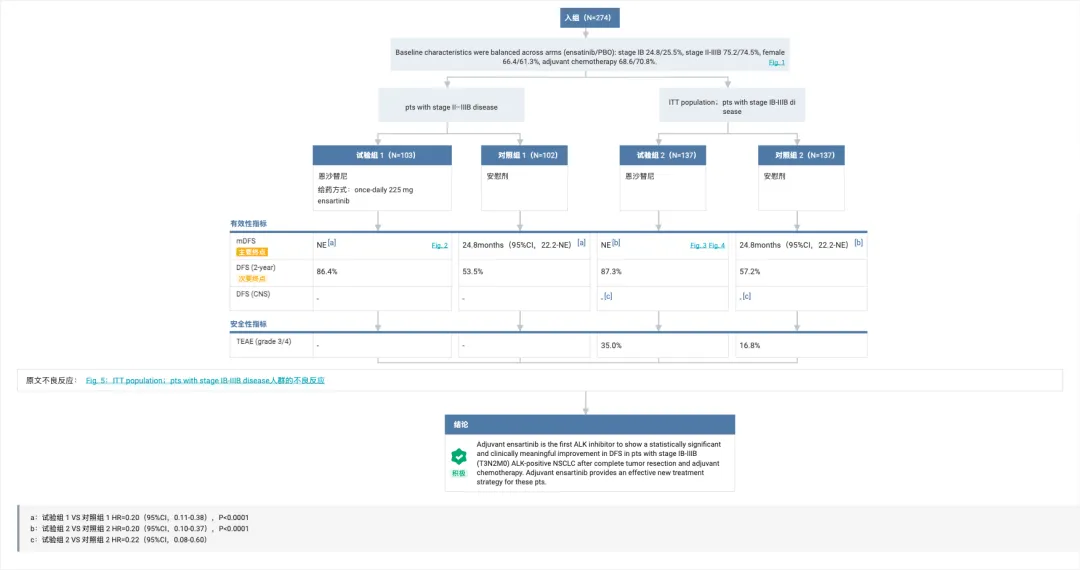
ELEVATE 是一项随机、双盲、安慰剂对照、多中心的 III 期临床试验。2022 年 7 月至 2024 年 7 月期间,共入组 274 例患者,随机分配至恩沙替尼组(n=137)和安慰剂组(n=137)接受治疗。截至数据截止日期(2025 年 6 月 26 日),研究中位随访时间为 22.1 个月。
来源:丁香园 Insight 数据库
结果显示,在 II-IIIB 期患者中,无病生存期(DFS)风险比(HR)为 0.20,其中恩沙替尼组患者 2 年 DFS 率达 86.4%,显著优于安慰剂组的 53.5%。在 ITT 人群中,DFS 风险比为 0.20 ,恩沙替尼组的 2 年 DFS 率为 87.3%,安慰剂组为 57.2%。
此外,在所有亚组中均观察到一致的 DFS 获益。在 ITT 人群中,研究还观察到具有临床意义的中枢神经系统(CNS)DFS 获益。
安全性方面,研究过程总共报告了 3 例(3/274)患者死亡,其中恩沙替尼组 1 例,安慰剂组 2 例。安全性特征与已知的恩沙替尼安全性特征一致。
恩沙替尼是一种新型强效、高选择性的新一代 ALK 抑制剂,是贝达药业和控股子公司 Xcovery 共同开发的自主创新药。该产品已在国内获批 2 项适应症:
用于此前接受过克唑替尼治疗后进展的或者对克唑替尼不耐受的ALK阳性的局部晚期或转移性 NSCLC 患者的治疗(即二线适应症);
用于 ALK 阳性的局部晚期或转移性NSCLC 患者的治疗(新增一线适应症)。
2024 年 12 月,恩沙替尼一线适应症获得美国 FDA 批准上市。2025 年 2 月,恩沙替尼一线适应症欧洲上市申报程序正式启动。2025 年 6 月,澳门药物监督管理局批准盐酸恩沙替尼胶囊上市。

 会员动态
会员动态
 维健医药
维健医药  2026-04-27
2026-04-27
 296
296

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-27
2026-04-27
 294
294

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-20
2026-04-20
 486
486
 热门资讯
热门资讯